2020 ESMO Asia与ESMO IO肝癌领域研究进展回顾( 二 )
由此可见 , 仑伐替尼联合PD-1抗体治疗HCC具有良好的疗效和耐受性 , 相比单药联合组具有更高的ORR , DCR和更长的PFS;真实世界中HCC患者的基线与随机对照研究(RCT)中患者的基线特征不同 , 可为临床使用联合疗法提供更多的数据支持 。
NO.4
(ESMO-Asia)LBA2 - 信迪利单抗联合贝伐珠单抗生物类似物对比索拉非尼一线治疗晚期肝细胞癌(ORIENT-32)
ORIENT-32研究对信迪利单抗联合贝伐珠类似物对比索拉非尼一线治疗晚期HCC进行了探索 。 纳入初治的不可切除或转移性HCC患者 , 随机2:1入组接受信迪利单抗+贝伐珠类似物(N=380)或索拉非尼(N=191)治疗 。 联合治疗组对比索拉非尼组疗效结果显示:mOS未达到vs 10.4个月 , p<0.0001 , 风险比0.569;两组12个月生存率为62.4% vs 48.5%;mPFS为4.6 vs 2.8个月 , p<0.0001 , 风险比0.565 。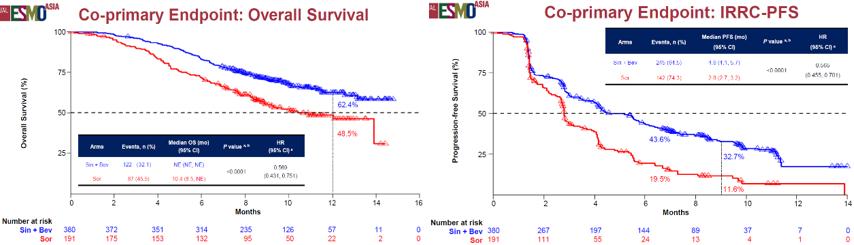 文章插图
文章插图
两组经独立委员会评估的ORR分别为20.5% vs 4.1% , P<0.0001 , 虽达到统计学差异 , 但联合治疗的ORR绝对数值差强人意 。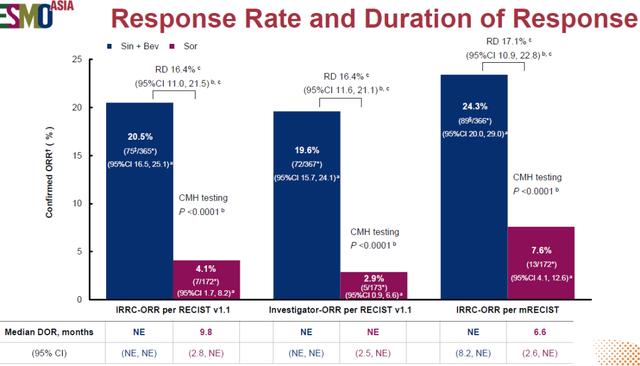 文章插图
文章插图
安全性方面 , 联合治疗组对比索拉非尼组3~4级AE发生率为54.5% vs 47.0% , 严重AE为32.4% vs 19.5% , 导致治疗中止或退出试验的比例也是联合组更高(49.5%、13.7% vs 40.5%、5.9%) 。
NO.5
(ESMO-Asia)170P - 信迪利单抗联合安罗替尼一线治疗晚期肝癌
此为一项单臂、Ⅱ期研究 , 纳入20例晚期不适合根治性手术和/或局部治疗的HCC患者 , 无既往系统治疗 , 接受信迪利单抗200mg D1 Q3W联合安罗替尼12mg D1-14 Q3W , 直至疾病进展或不耐受 。 14例可评估患者的结果显示:ORR 42.9%(1例CR、5例PR) , DCR 92.9% 。 mDOR尚未达到 。 6个月PFS率为78.8% , mPFS及mOS均尚未达到 。 如下图所示 。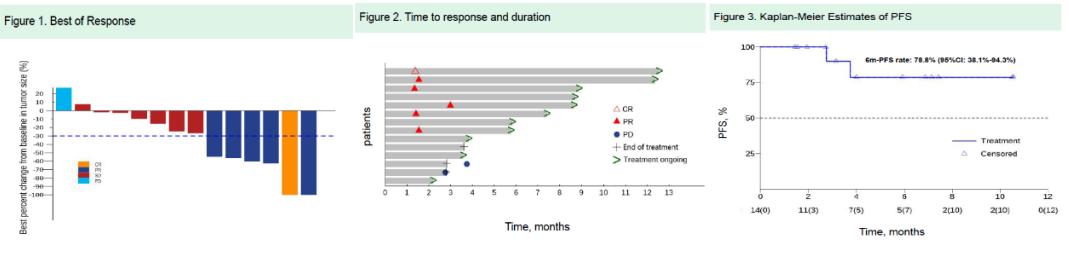 文章插图
文章插图
该联合方案中位治疗时间为5.3个月 。 安全性上 , 最常见治疗相关不良事件(TRAE)为1-2级 , 无4/5级TRAE发生 。 7例患者需降低安罗替尼剂量(4例降到10mg , 3例降到8mg) 。 TRAE未导致治疗终止 。
金风玉露一相逢-HCC免疫/靶向治疗与局部治疗强强联合
NO.1
(ESMO-Asia)171P-TACE+仑伐替尼对比TACE+索拉非尼治疗伴门静脉癌栓(PVTT)的肝癌患者
这是一项开放、单中心、前瞻性、随机对照研究 , 探索了经肝动脉化疗栓塞术(TACE)联合仑伐替尼对比TACE联合索拉非尼治疗伴PVTT(I-IV型)的不可切除HCC患者的疗效和安全性 。 本研究入组64例未经治疗的晚期HCC患者 , 以1:1比例随机分配至TACE+仑伐替尼组(n=32)和TACE+索拉非尼组(n=32) 。 结果显示 , TACE+仑伐替尼组患者的中位肿瘤进展时间(mTTP)显著长于TACE+索拉非尼组(4.7个月vs 3.1个月 , P=0.041) 。 TACE+仑伐替尼组的mOS在数值上更优于TACE+索拉非尼组(14.5个月vs10.8个月P=0.18) 。 TACE+仑伐替尼组的ORR显著高于TACE+索拉非尼组(53.1% vs 25.0% , P=0.039) 。 两组治疗相关的严重不良事件(n=5 vs 4) , 包括4例胃肠道出血和5例腹部感染 , 两组的停药和减少药物剂量的发生率相似 , 且在研究期间没有出现治疗相关的死亡 。
TACE+仑伐替尼组和TACE+索拉非尼组的TTP(A)和OS(B)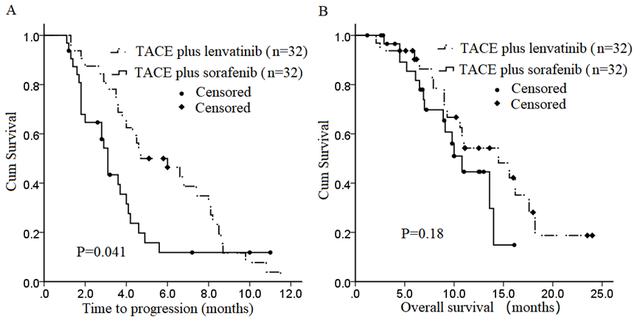 文章插图
文章插图
NO.2
(ESMO-Asia)172P-仑伐替尼、特瑞普利单抗和HAIC三药联合方案 , 对比仑伐替尼单药治疗晚期HCC的疗效和安全性
这是一项回顾性真实世界研究 , 旨在评价仑伐替尼、特瑞普利单抗和肝动脉灌注化疗(HAIC)三联方案 , 对比仑伐替尼单药方案一线治疗晚期HCC的疗效和安全性 。 研究共纳入157例晚期HCC患者 , 分别接受仑三药联合方案(N=71)或伐替尼单药(N=86)治疗 。 研究结果显示 , 三药联合组有更长的PFS(11.1个月vs 5.1个月 , p
- 李勇教授:2020中国动态血压监测指南解读
- 最新版「北大核心期刊目录(2020版)」之医药、卫生门类
- 张瑞岩教授:2020 AHA/ACC肥厚型心肌病诊断及治疗指南解读
- 2010-2020,肿瘤试验设计和结果发生了哪些重大变化?
- 《中国2型糖尿病防治指南(2020版)》要点提示,一文全知道!
- 每年都体检,却查出晚期癌症?!
- OCC 2021丨周京敏教授:2020心肌梗死后心力衰竭防治专家共识解读
- 陆国平教授:2020-2021血脂领域有这些新进展!丨OCC 2021
- 《中国吸烟危害健康报告2020》发布!烟草引发5大疾病,你还抽?
- 《中国吸烟危害健康报告2020》发布,吸烟人数超3亿!该保养
