国内首个!浦东企业开启肿瘤免疫治疗新征程
1月7日 , 国家药品监督管理局药品审评中心(CDE)官网最新公示 , 位于张江科学城的恒润达生1类生物新药抗人CD19-CD22 T细胞注射液获得临床试验默示许可 , 拟开发用于复发/难治B细胞急性淋巴细胞白血病 。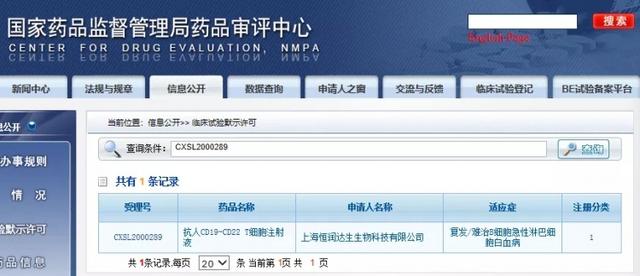 文章插图
文章插图
CDE官网信息显示 , 恒润达生申报的“双靶点T细胞注射液治疗急性B淋巴细胞白血病的临床前研发”是国内首个立项的“双靶点”研发项目 。
“抗人CD19-CD22 T细胞注射液”是一种针对CD19-CD22靶点的基因工程修饰的自体CAR-T细胞制品 , 其作用机理是经病毒载体体外基因工程修饰 , 使得T细胞携带CD19和CD22二元CAR元件 , 该种基因改造的T细胞能特异性地识别B细胞表面的CD19和/或CD22分子 , 从而使得该产品有望更加彻底的清除体内的肿瘤病灶 , 有效降低CAR-T治疗后的复发概率 。
急性淋巴细胞白血病(Acute lymphoblastic leukemia , ALL)是一类起源于前体B或T淋巴前体细胞在骨髓、血液、髓外的恶性增殖性肿瘤 , 其中B-ALL约占80% , T-ALL约占20% 。 嵌合抗原受体(CAR)的T细胞可有效识别肿瘤抗原 , 引起特异性抗肿瘤免疫应答 , 目前被认为是针对恶性血液肿瘤的最有希望的治疗手段 。
据恒润达生方面介绍 , 该产品的申报从2020年10月16日获得CDE受理 , 10月20日承办之后 , 仅仅用了两个月的时间即获得临床试验默示许可 。 至此 , 恒润达生已获四张临床批件 , 在国内细胞治疗行业中一马当先 。 其中三个批件的注册临床同步在国内知名三甲医院开展 , 是国内启动CAR-T注册临床试验最多的企业之一 。
栏目主编 许素菲
责任编辑 刘婉鑫
实习编辑 杨林雨
【国内首个!浦东企业开启肿瘤免疫治疗新征程】图片来源 资料图
- 心衰治疗里程碑突破!首个miRNA药物证明安全有效!
- NB封面文章:首个全国急性播散性脑脊髓炎的发病率调查
- AADvac1:首个阿尔兹海默症疫苗II期临床结果积极
- 60年首个国产新药获批!红斑狼疮进入生物治疗时代
- 国内眼科临床医生缺口巨大 专家吁加强实操培训
- 极具争议!17年来首个老年痴呆症新药被批准上市
- 国内首款ADC药获批,荣昌借此杀入胃癌赛道,此外它还瞄着PD1的“大后方”
- NEJM:KRAS突变肺癌的救星!首个靶向药sotorasib临床II期研究数据更新,患者生存期超过一年丨临床大发现
- 广谱且精准,Larotrectinib即将国内上市,NTRK抑制剂开辟广谱抗癌热潮
- FDA一再打破常规,在“首个”阿兹海默病新药上市过程中……
