基石药业、微芯生物、迪哲药业的3款新药拟纳入突破性治疗品种
【基石药业、微芯生物、迪哲药业的3款新药拟纳入突破性治疗品种】近日 , 中国国家药监局药品审评中心(CDE)公示 , 三款新药拟纳入突破性治疗品种 , 分别是:Blueprint Medicines/基石药业RET抑制剂BLU-667胶囊(pralsetinib , 普拉替尼) , 微芯生物多靶点多通路选择性激酶抑制剂西奥罗尼胶囊 , 迪哲医药EGFR抑制剂DZD9008片 。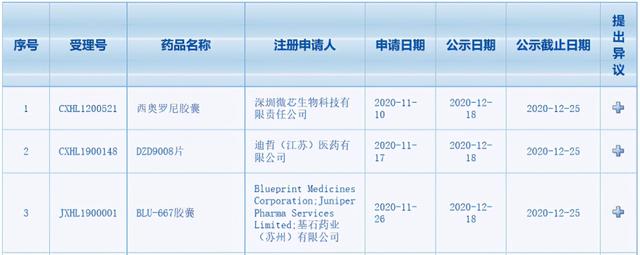 文章插图
文章插图
来源:CDE官网
其中 , 普拉替尼由基石药业合作伙伴Blueprint Medicines公司开发 , 是一种口服、每日一次、强效高选择性RET抑制剂 , 是每日一次的口服精准疗法 。 基石药业于2018年6月获得了该产品在大中华区的独家开发和商业化授权 。 今年7月 , Blueprint Medicines还与罗氏(Roche)开展全球(除大中华地区之外)合作 , 以开发及商业化用于治疗RET突变癌症的普拉替尼 。
CDE公示信息显示 , 普拉替尼纳入“突破性治疗药物品种”的拟定适应症为转染重排(RET)突变阳性的晚期或转移性甲状腺髓样癌(MTC)患者的系统性治疗 。 根据药物临床试验登记与信息公示平台 , 基石药业正在中国开展一项BLU-667治疗甲状腺癌、非小细胞肺癌(NSCLC)和其他晚期实体瘤患者的1期研究 。 此次纳入预期将加快该款新药在中国的临床审评和上市速度 , 尽早为国内患者带来福音 。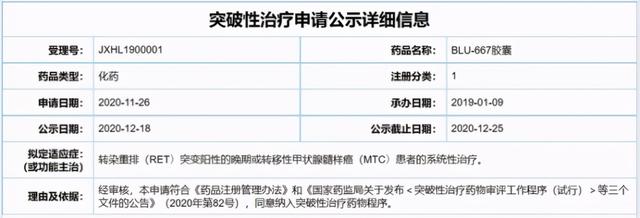 文章插图
文章插图
在我国 , 甲状腺癌发病率逐年上升 。 相关报告显示 , 甲状腺癌发病率约为14.6/10万人 , 其中甲状腺髓样癌(MTC)发病率约占甲状腺癌的2%-4% , 其恶性程度较高 , 易发生远处转移 , 且晚期患者疗效不佳 。 约60%的甲状腺髓样癌可检测出RET基因突变 , 晚期患者的RET突变比例更高达90% 。 创新靶向药普拉替尼的“诞生”打破了甲状腺髓样癌(MTC)多靶点“撒网”的局面 , 它可以高选择性、精准打击RET突变基因 , 对携带RET突变的甲状腺髓样癌(MTC)晚期患者具有更广泛和持久的抗肿瘤作用 , 而且通过抑制原发和继发突变 , 普拉替尼有望克服和预防临床耐药的发生 。
业界普遍认为 , 建立突破性治疗药物审批通道的意义在于 , 通过早期临床数据发掘优势产品、集中多方资源重点研发、缩短优势产品研发周期 , 提高成功获批的数量 , 减少止步于临床前的新分子实体的数量 , 从而让患者早日获得更好的治疗 。 当前 , 突破性疗法俨然已经成为药物获批风向标 , 代表着药物研发的最新突破 。
此外 , 美国食品药品监督管理局(FDA)之前已授予普拉替尼“突破性疗法认定” , 本月初 , FDA加速批准普拉替尼扩展适应症 , 用于治疗携带RET变异的甲状腺癌患者 , 包括12岁以上需要全身治疗的晚期或转移性RET突变甲状腺髓样癌MTC患者 。
- 张伯礼院士担任悦康药业创新药Ⅲ期临床试验DMC主席
- 红日药业重金布局中药颗粒产业 中药颗粒将迎黄金时代
- 基石药业-B:舒格利单抗拟上市,大适应症下PD-(L)1的重磅玩家
- 例例声辉|不可切除局晚期NSCLC在放化疗的基石上加一剂猛药
- 连花清瘟胶囊卖到脱销的以岭药业
- 扬子江药业匠心人物六——张敏:身手敏捷的设备“医者”
- 以岭药业:连花清瘟获乌兹别克斯坦药物注册批文
- 聚焦名中医!平安好医生与天江药业达成战略合作
- 平安好医生与天江药业达成战略合作,开启互联网+中医药新模式
- 连花清咳片获批进入新版医保目录,有望成为以岭药业新的业务增长点
