「新冠病毒」最新研究驳斥新冠病毒为“人造”产物 蛇不是中间宿主( 二 )
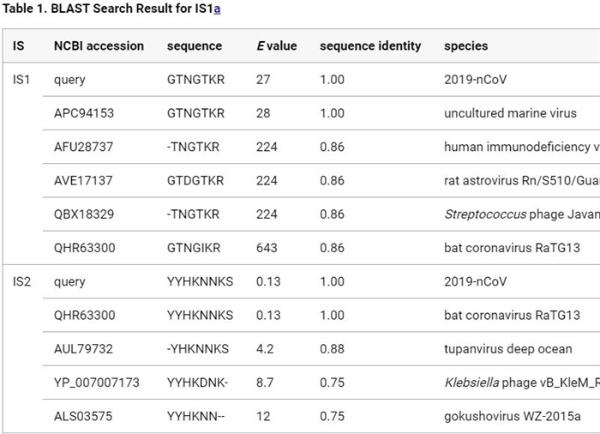
在研究这四个插入片段的病毒同源性时,研究人员通过非冗余序列数据库(NR)对其进行BLAST序列搜索,将搜索结果限制为病毒(taxid: 10239),但将其他搜索参数保留为默认值。表1列出了为每个插入片段的前5个序列同系物(包括查询本身)。
之前的说法认为这四个插入片段是2019-nCoV和HIV-1所独有的,然而所有四个插入片段都可以在其他病毒中找到。事实上,HIV-1蛋白在四个插入片段中只有一个是最常见的,而四个插入片段中有三个是在蝙蝠冠状病毒RaTG13中发现的。
文章图片

文章图片
此外,部分由于这些插入片段的长度很短, 6到8个氨基酸, BLAST的E值(BLAST所使用的参数评估统计学意义的排列,通常需要< 0.01被认为是重要的)几乎都是> 4,除了蝙蝠冠状病毒IS2。这些高E值表明,这些相似性中的大多数可能是巧合。
考虑到四个插入片段中有三个是在蝙蝠冠状病毒RaTG13中发现的,很容易假设这些“插入”可能是直接遗传自蝙蝠冠状病毒。目前,至少有7个已知人类冠状病毒(2019-nCoV、 SARS-CoV、MERS-CoV、HCoV-229E、 HCoV-OC43、 HCoV-NL63和HCoV-HKU1),其中许多病毒,包括SARS-CoV和MERS-CoV被认为是从蝙蝠传播的。
为进一步检查2019-nCoV和蝙蝠冠状病毒之间的进化关系,与其他人类冠状病毒相比,研究人员利用MUSCLE创建了一个多重序列比对(MSA),呈现在图3中,对于所有七种人类冠状病毒和两种蝙蝠冠状病毒,RaTG13和RsSHC014,它们分别被认为是2019-nCoV和SARS-CoV的祖先。
在2019-nCoV的四个“插入片段”(IS)中,IS1仅具有一个不同于蝙蝠冠状病毒的残基,并且七个残基中的三个与MERS-CoV相同。 IS2和IS3都与蝙蝠冠状病毒相同。
对于IS4,虽然BLAST的局部序列比对没有击中表1中的蝙蝠冠状病毒,但它与MSA中的蝙蝠冠状病毒有密切的进化关系。特别是,2019-nCoV的IS4片段“QTQTNSPRRA”中的前6个残基与RaTG13相同,而蝙蝠冠状病毒或SARS-CoV中缺失的后4个残基与MERS-CoV和HCoV-HKU1至少有50%的同源性。
由此,研究人员认为2019-nCoV与蝙蝠冠状病毒RaTG13之间存在密切的进化关系,Pradhan等人在突刺蛋白中强调的四个插入位点并不是2019-nCoV和HIV-1所独有的。事实上,在这些非常短的片段上建立的序列比对的相似性在统计学上是不显著的,这是通过BLAST E值来评估的,而这种相似性在许多其他病毒中也存在,包括蝙蝠冠状病毒。从结构上看,这些“插入”远离了与ACE2受体结合的突刺蛋白的结合界面,如图2所示,这也与Pradhan等人的结论相矛盾。
2. 相对同义密码子使用度不能识别冠状病毒的中间宿主
另一项由Wei Ji等人进行的早期研究试图理解2019-nCoV的感染。在这项研究中,作者分析了2019-nCoV和八个脊椎动物的RSCU(相对同义密码子使用度,包括两种蛇(银环蛇和眼镜蛇)、西欧刺猬、中华菊头蝠、土拨鼠(旱獭)、马来西亚穿山甲、鸡 (普通家鸡),和人类(智人)。在这些脊椎动物中,与2019-nCoV相比,蛇的密码子使用差异最小,因此Ji等人提出,蛇是2019-nCoV的中间宿主。
然而,由于缺乏先前的人畜共患冠状病毒可以感染哺乳动物和鸟类以外的动物的生物学证据,这一结论在病毒学家中引起了争议。
此外,最近的研究显示,初步证据表明,穿山可能是类似2019-nCoV的冠状病毒的宿主,进一步证明Ji等人的结论无效。虽然关于蛇是中间宿主的结论一直受到科学界的普遍质疑,但是仔细检查RSCU方法的基础和可靠性仍然很重要,这将有助于防止这种有偏见的分析误导科学界和公众。在最新研究中,我们通过对RSCU分析的大规模复制,仔细研究了生物信息学方法和潜在的生物学假设。
如图4A所示,蛇并不是RSCU距离2019-nCoV最小的脊椎动物,这说明Ji等人对RSCU分析的实施是不完整的。更重要的是,图4中的数据显示,与冠状病毒传播无关的动物,如青蛙和蛇,与所有三种冠状病毒已知宿主的RSCU距离始终较小。
- 健康界■第二版)来了,新型冠状病毒肺炎重型、危重型病例诊疗方案(试行
- 健康零距离■最新!广州市卫健委通报“外籍患者咬伤护士”:已对该护士进行会诊
- 「前瞻网」有制造商检测试剂盒已被禁止出口,英国大规模新冠抗体检测正逐步推进
- 「半岛晨报」李兰娟:新冠肺炎发病第二周是病情进展关键窗口
- [健康直通车]为什么德国新冠死亡率低于其他国家?
- 『健康零距离』新冠病毒或将蔓延到原始丛林深处!巴西亚马逊雨林首个原始部落居民确诊新冠
- 最新娱乐新闻关注:64岁健身女王居然带儿子上杂志封面?网友:还以为他们是情侣!
- 福建闽南网@系从美旅行返台,嘉义出现首例新冠肺炎确诊病例
- #临沂河东#最新!青岛新增1例!报告为无症状感染!
- 好医生官方■突发伤医事件!广州外籍新冠肺炎确诊患者殴打女护士!
