文章插图
诊断后6个月内MRD转阴表明MRD转化和未来临床复发的可能性更高
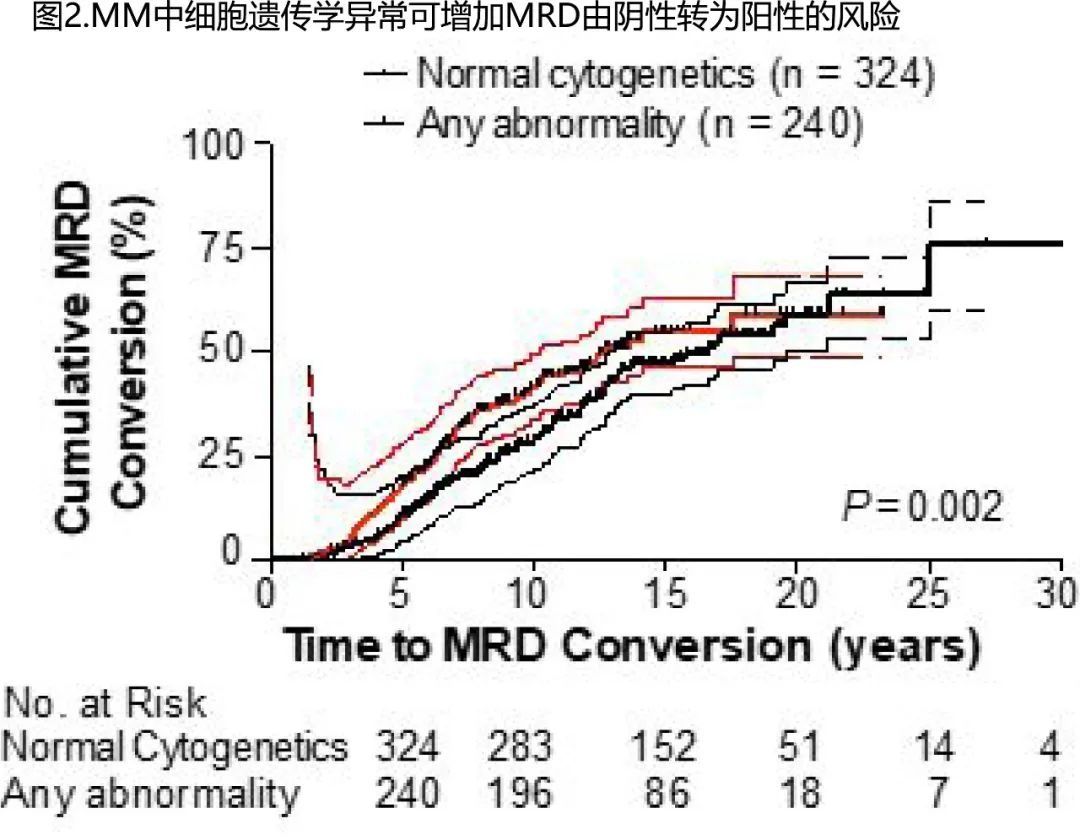
作者探索了复发的时间和模式与MRD转换的关系,以确定初始获MRD阴性是否预示着后续的临床复发,以及至MRD转阴时间是否影响后续MRD转换。
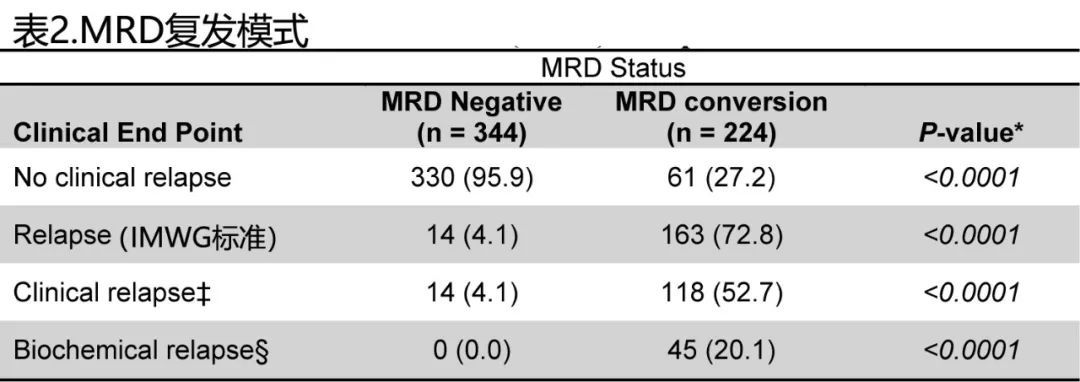
正如所预期的那样,MRD转换与复发风险增加强烈相关,而维持MRD阴性则预示着避免复发(73%, 163/224 vs. 4%, 14/344; RR,3.5; P < 0.0001, 表2; 图3A),且MRD阴性临床复发的4%患者中,MRI 和/或PET-CT扫描下均存在大病灶,但骨髓随机检测中均未呈现微小骨髓瘤浸润。
文章插图
文章插图
在163例MRD转换且后续复发的患者中,多数为临床复发(118/163; 72%),仅剩下少数为生化复发28% (45/163),见表2。临床/生化复发在MRD转换患者中的比例明显高于MRD持续阴性患者(分别为53%, 118/224 vs. 4%, 14/344; P < 0.0001 和20%, 45/224 vs. 0%, 0/344; P < 0.0001,, 表2)。MRD阴性丢失到临床复发的中位时间为1年,到生化复发的中位时间为0.5年。
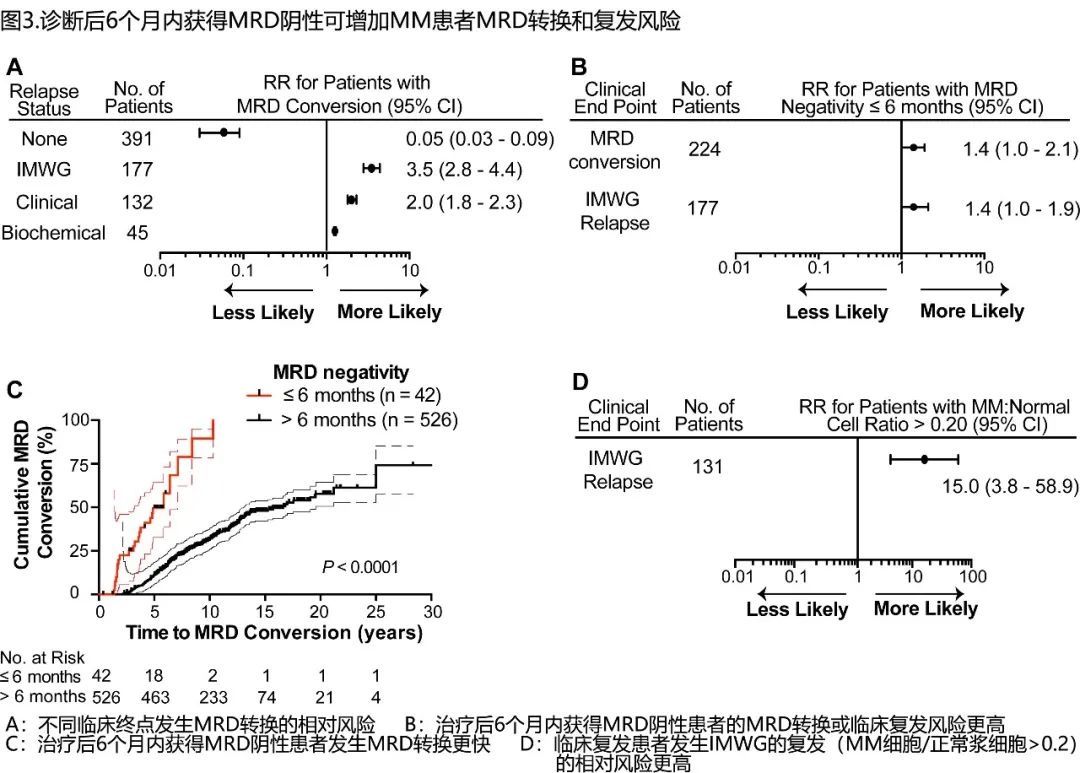
需要注意的是,224例MRD转换的患者中有61例(27%)未发生临床复发,且其中多为GEP70 亚型的CD2 和HY(CD2, n = 20; HY, n = 20)。并且极为有意思的是,早期(治疗后6个月内)MRD转阴竟与MRD转换风险增加(57%, 24/42 vs. 38%, 200/526; P = 0.02)和IMWG复发风险增加相关(50%, 21/42 vs. 29%, 156/526; P = 0.009),见图3B。此外,MRD早期转阴患者至MRD转换的时间也较短(P <0.0001; 图3C)。
MRD转换水平也可预测复发的临床表型。作者使用流式细胞术测定的异常浆细胞与正常浆细胞的比值>0.20作为临界值,骨髓中达到该阈值的患者临床复发风险可增加15倍(RR=15.0;95%CI,3.8-58.9;P < 0.0001;图3D)。此外,47例NGF和影像学MRD阴性的患者NGS也显示MRD阴性,NGS和NGF之间的阴性一致性为47%(22/47),其余病例为NGF阴性但NGS阳性(53%,25/47;NGF-/NGS +)。在NGF-/NGS + MRD阴性的患者中未发生临床复发。
MRD远期转换患者OS较好,接近MRD持续阴性患者
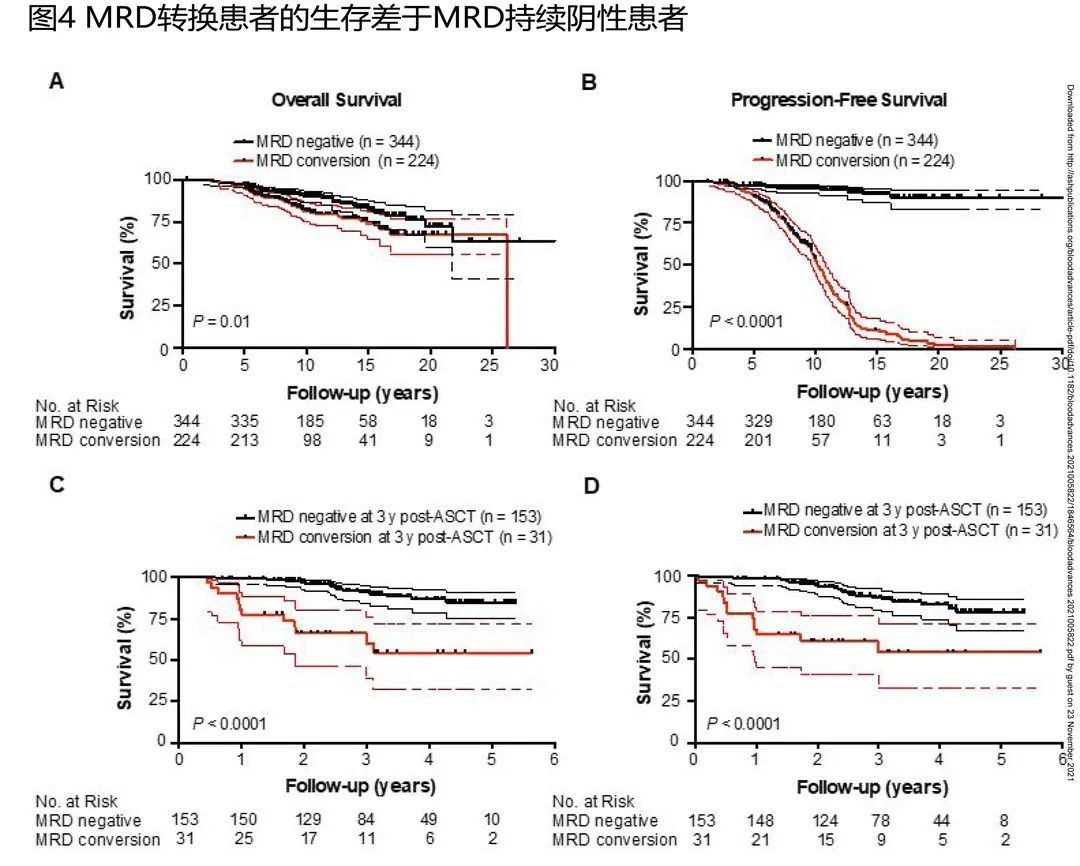
与整个队列相比,发生MRD转换患者的OS和PFS较差(OS: HR=1.7; 95% CI, 1.1 – 2.7, P = 0.01 ;PFS: HR=18.9;95% CI, 13.2 – 27.0, P < 0.0001; 图4A-B),当然,作者认为这并不意外。从诊断计算,MRD转换患者的中位PFS和OS分别为10.2和26.2年,而MRD持续阴性患者的中位PFS和OS均为达到,10年PFS和OS率为88%和90%。
文章插图
为避免MRD时间转换带来的时间偏差,作者从ASCT开始计算,选择ASCT后3年作为里程碑,发现MRD转换仍对PFS和OS有负面影响(OS: HR, 5.7; 95% CI, 6.3 – 63.0, P < 0.0001; PFS: HR, 4.5; 95% CI 4.3 – 33.7, P <0.0001; 图4C-D)。但5年后MRD转换的负面影响便消退 了(OS: HR, 1.4; 95%CI, 0.6 – 3.6; P = 0.47; PFS: HR, 1.0; 95% CI, 0.5 – 2.0; P = 0.96)。
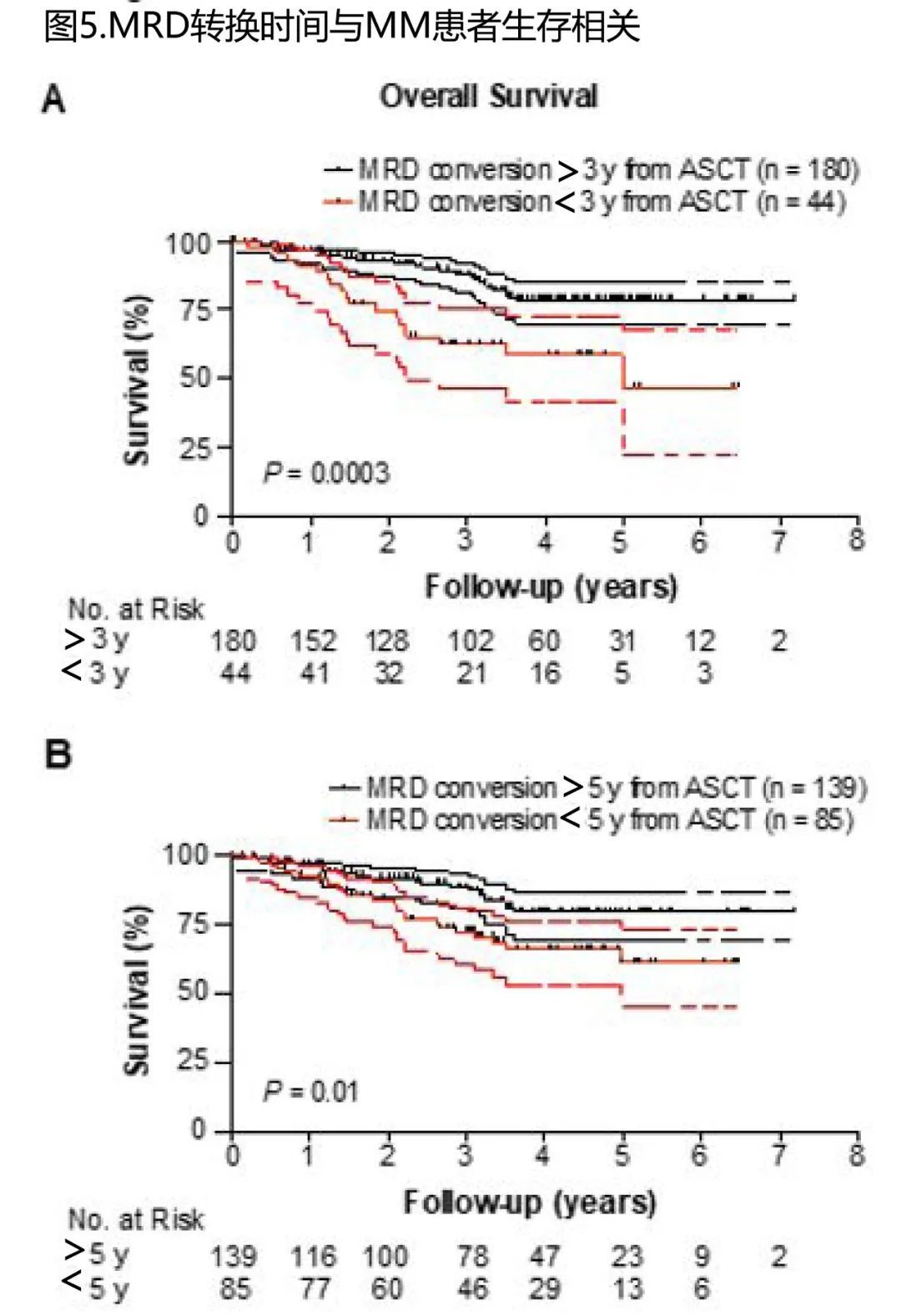
为评估MRD转换的时间是否影响患者预后,作者根据首次ASCT的临界值对MRD转换阳性的患者进行了分组,然后根据MRD转换时间进行随访。发现首次ASCT后≤3年发生MRD转换的患者的OS显著低于首次ASCT后>3年发生MRD转换的患者(HR=2.8;95%CI 1.8-8.2;P = 0.0003;图5A)。尽管程度较轻,但对患者在首次ASCT后 < 5年和≥5年分层时,这种时间依赖性MRD转换对OS的影响持续存在(HR=2.1; 95%CI 1.2 – 4.0; P = 0.01; 图5B)。
文章插图
讨论
本研究共纳入568例MRD阴性患者且进行了长期随访,还整合了PET-CT、MRI DWIBS以及骨髓MRD,证实相当一部分MM患者(39%)中在MRD阴性后会发生MRD转换,MRD转换中位1.0年后发生临床复发。
MRD演变的动力学模式比单次MRD检测可提供更多信息。正如预期那样,在相当大比例(93%)的低危MM患者中可实现持续的MRD阴性。
大多数MRD转换患者(76%,170/224)发生于初次诊断后10年内,ASCT后至MRD转换的中位时间为6年,这表明MRD转换多发生在作者中心常规的标准3年三药维持治疗之后。MRD转化的风险在诊断后5年内要高得多,虽然随着时间的推移而降低,但风险仍可持续至诊断后15年。
在诊断后10年时仍为MRD阴性的患者中,后续MRD转化风险较低(31%)。此外,MRD转换的患者中有70%发生了临床复发,MRD转换的患者中有29%为PET/MRI阳性,因此再次强调了新型影像学技术和骨髓MRD评估的重要性,尤其是在复发情况下。
应注意的是有27.1%的MRD转换患者未发生临床复发,且多为CD2和HY GEP亚型。因此,从CR转化为具有稳定残留MRD克隆的MGUS样状态(可与骨髓微环境共存,无临床后果)貌似可行。关于GEP亚型中CD的预后价值,本研究与既往报道貌似有差异,报道认为GEP亚型CD2的CR率和MRD阴性率最低,但与CD1(CR率最高的亚型)的临床预后相当。此外,CD2亚型可能发生远期复发,而其先驱便是MRD转化,但仍然具有良好的总体预后。
- 医保|创新药实现医保报销 助力多发性骨髓瘤慢病化
- 多发性|宫氏话健康丨多发性硬化症,女性发病率比男性高一倍
- 多发性骨髓瘤|浅谈多发性骨髓瘤的规范化治疗
- 多发性|永州市中心医院成功开展全市首例感觉诱发电位检查
- 肾功能|腰腿疼须警惕多发性骨髓瘤
- 多发性|一月注射一次,多发性硬化新药获批上市
- 奥法妥木单抗获批,多发性硬化治疗进入精准治疗时代|健康 | 硬化
- 血液科|出现不明原因腰腿痛应重视 江苏省中医院专家成功控制多发性骨髓瘤患者病情
- 手游|幻书启示录宣布关服,绊爱无限期停止活动 | 二次元周报
- 多发性肌炎|体内有癌,手脚知道?四肢出现4个异常,警惕肺癌来敲门
