新药正式在中国获批了第一款获得国际认可的本土抗癌新药( 三 )
同时 , 在临床试验中 , 泽布替尼也显示出了更好的安全性!如果癌症变成了慢性病 , 患者需要长期服用药物 , 安全性也变得至关重要 。
4
下一站 , 更多适应症 , 更多国家
对于MCL这个适应症 , 泽布替尼在获得中美两国的上市批准之后 , 也于近期在以色列提交了上市申请 。 同时 , 泽布替尼也在寻求欧洲上市的机会 。 但是泽布替尼不仅仅是一个用来治疗MCL的药物 。
就在5月底 , 百济神州在今年的ASCO大会上公布了泽布替尼对华氏巨球蛋白血症(WM)患者治疗3期临床试验的更新数据 。 这不是一个简单的3期研究 , 而是与伊布替尼的头对头比较 , 目的在于证明到底谁更好 。 伊布替尼是最先获得批准的一代BTK抑制剂 。 所以 , 这个研究 , 也是中国本土新药首次与国外药企重磅药所展开的头对头优效性临床试验 。
这项随机、开放标签的国际多中心3期临床试验 , 在欧洲、澳大利亚和美国的61个中心开展 , 先后纳入了229例WM患者 , 是全球范围内迄今为止针对WM治疗的最大规模的3期临床试验 。 研究结果显示 , 在所有患者中 , 根据研究者在随访时间为24.2个月时对主要指标进行的评估 , 泽布替尼治疗后有30.4%的患者获得了完全缓解(CR)或非常好的部分缓解(VGPR) , 而伊布替尼治疗组只有18.2%的患者达到这个指标 , 泽布替尼取得了优于伊布替尼的缓解率(p= 0.0302) 。
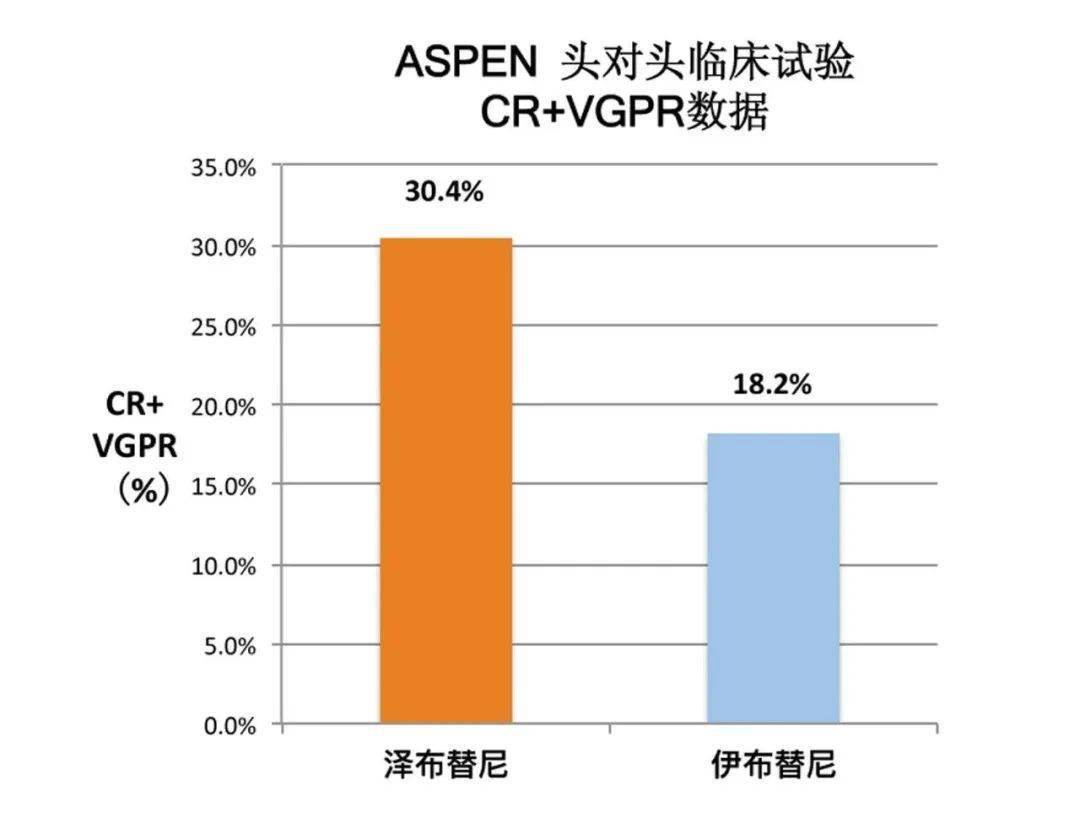
文章图片
华氏巨球蛋白血症等B细胞淋巴瘤的患者一般年纪比较大 , 平均发病年龄为70岁 , 所以药物的安全性和耐受性也是非常值得关注的问题 。 与此前公布的研究数据所展现的趋势一致 , 泽布替尼在安全性方面也取得了比伊布替尼更好的表现 。 尤其是房颤这类需要特别关注的不良反应 , 泽布替尼和伊布替尼的发生率分别为3.0%和18.4% , 可以看出泽布替尼的安全性大大提高了 。
对于华氏巨球蛋白血症适应症 , 目前泽布替尼已经获得美国FDA授予的快速通道资格 , 未来将有机会提交该适应症的申请 。
泽布替尼的用途可能还不仅仅是癌症 , 还可能与新冠有关 。 在治疗华氏巨球蛋白血症患者的过程中 , 波士顿达纳-法伯癌症研究所的医生发现 , 6个使用泽布替尼治疗的华氏巨球蛋白血症患者 , 在感染新冠病毒后都没有出现大事 。 目前认为新冠病毒感染后所激发免疫细胞因子风暴 , 是导致病情严重的原因 , 而BTK抑制剂有可能也有抑制细胞因子风暴的作用 。 基于这个发现 , 泽布替尼已经启动治疗新冠肺炎的2期临床试验 。 由于目前中国疫情已经基本控制住了 , 泽布替尼治疗新冠的临床试验只能在美国开展 。
期待泽布替尼后续的临床试验 , 能继续带来惊喜 。 但眼下 , 最重要的是 , 对于中国的癌症患者来说 , 使用泽布替尼治疗不再只是希望 , 而是成为现实了 。
如果这个本土新药的定价能低一点 , 也早一点进入医保 , 那现实会更美好一点。

文章图片
延伸阅读:
【新药正式在中国获批了第一款获得国际认可的本土抗癌新药】(作者:张洪涛 , 笔名“一节生姜” 。 宾夕法尼亚大学医学院病理及实验医药系研究副教授 , 研究领域:癌症的靶向治疗以及免疫治疗 。 著有科普读物:《吃什么呢?——舌尖上的思考》 , 《如果舌尖能思考》 。 可以谈最前沿的医学研究 , 也可以讲最通俗的故事 。 )
- 旗袍|周涛越活越年轻了!穿一套中国风旗袍,优雅大气迷人!
- 中国共产党|无私奉献科学报国|北京协和医院内科援藏援疆代表座谈共话家国情
- 专科|行业彰显现实力 成绩斐然传佳讯——“2020届中国中医医院最佳专科” 东直门医院再上榜
- 美丽|中国最具特色的峡谷,被誉为“地球最美丽伤痕”,拥有72条瀑布
- 无声情话|安徽将增一“巨无霸”机场,预计2021年正式通航,这个城市有福了
- 董睿博宇|官宣!CBA超级外援正式离队,新疆男篮签下他能再度冲冠
- 汇景|著立郴江,入境江湖 |汇景·雍和居案名正式发布
- 试验|巴西暂停测试中国新冠疫苗,科兴生物回应:仍在沟通了解中
- 剧情|治愈剧《遇见你》正式开机 一同驰骋美好时光
- 至今|世界上最厉害的2个烂尾楼,一个至今136年没建完,一个在中国!
