医学前沿传播者
Connecting Doctors & Sharing Better
iCardioOncology
01
背景
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是临床最常见的肺部慢性炎症性疾病,是全球致残及致死率较高的疾病之一。气流受限是COPD的主要病理生理特征,也是反映疾病严重程度的指标,但它对死亡率的预测价值有限。 白介素33(IL-33)是IL-1家族成员,具有高度致炎性,近年来收到了广泛关注。生长刺激表达基因2蛋白(ST2)是IL-33的受体,主要分为跨模型(ST2L)和可溶性(sST2)两种表达亚型。研究表明IL-33可通过与ST2L结合激活单核巨噬细胞,扩大炎症反应,而sST2竞争性与IL-33结合,以达到拮抗炎症反应的作用。
目前sST2作为心衰诊疗的生物学标志物已被临床广泛运用,但在COPD患者中少有报道。本研究旨在比较慢性阻塞性肺疾病(COPD)患者和健康对照者sST2和IL-33水平,评估sST2对COPD患者长期预后的预测价值。
02
方法
在这项前瞻性队列研究中,COPD患者纳入标准包括年龄在40岁以上、至少20年的吸烟史和经螺旋测量证实的气流受限。
对照组包括吸烟和不吸烟的人,比例为3(COPD):1(吸烟):1(不吸烟)。对照均为年龄匹配,测量有无气流限制迹象。
主要终点为COPD稳定期患者任何原因死亡的时间。
对每个参与者进行体检,包括体重指数(BMI)、血压、心率和6分钟步行试验(6-MWT)。按照欧洲呼吸学会和美国胸科学会的标准,用肺活量测定法和体容积描记法检测肺功能。晨起空腹状态下从受试者的眼眶窝取静脉血标本。
所有统计分析均采用SPSS 22.0和STATA版本12。
【 慢性阻塞性肺疾病|ST2与慢性阻塞性肺疾病患者的全因死亡率】 03
结果
3.1. 基本特征
研究组在年龄、性别和BMI方面具有可比性,心率、CRP、中性粒细胞计数差异有统计学意义(表1)。所有研究组NT-proBNP水平均低于80ng/L。
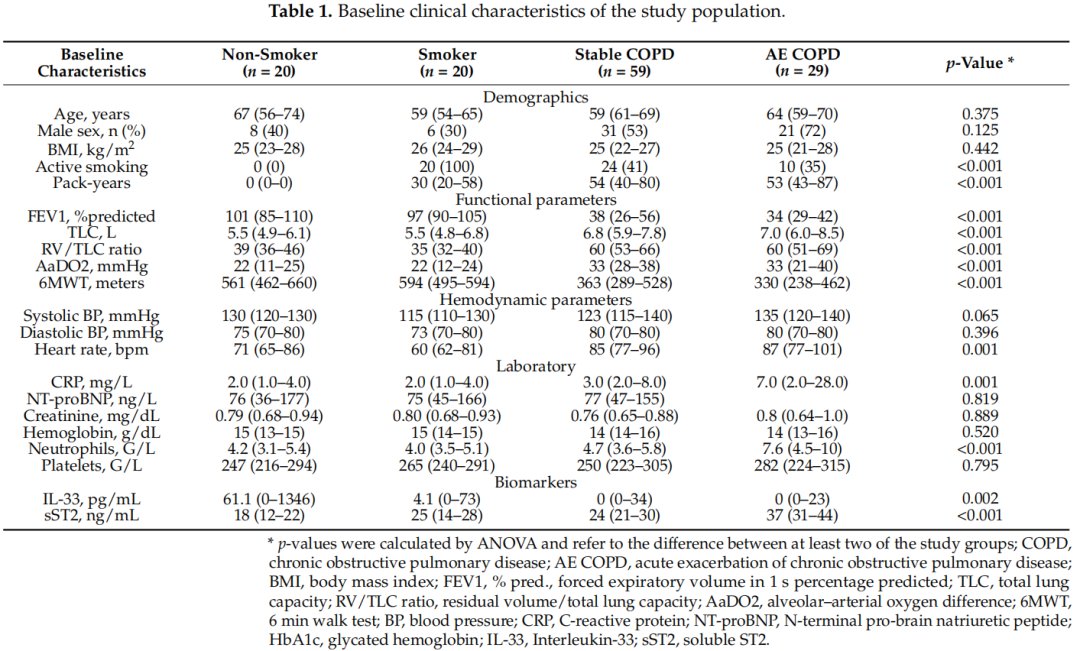
文章插图
3.2. IL-33, sST2与COPD的决定因素
COPD与非吸烟对照者sST2水平总体较高(24.2ng/mL、IQR 20.6~30.2 vs. 18.1ng/mL、IQR 11.9~22.2,p=0.005,图1A),随着GOLD阶段水平升高而升高(图1C)。急性加重的COPD患者与稳定期COPD相比,sST2水平升高(39.59ng/mL、IQR 31.77~44.33 vs. 24.2ng/mL、IQR 20.6~30.2,p=0.001 , 图1E)。急性加重后,循环sST2浓度与急性加重相比,恢复到基线水平(24.36ng/mL、IQR18.8~30.3,p=0.004,图1E)。
COPD患者无论疾病严重程度都与IL-33水平具有可比性(GOLD 2: 0pg/mL、IQR 0~99.12 vs. GOLD 3: 0pg/mL、IQR 0~74.67 vs. GOLD 4: 0pg/mL、IQR 0~0.55,p=0.185,图1D)。
36例(61%)COPD稳定期患者IL-33低于检测限,21例(72%)加重。
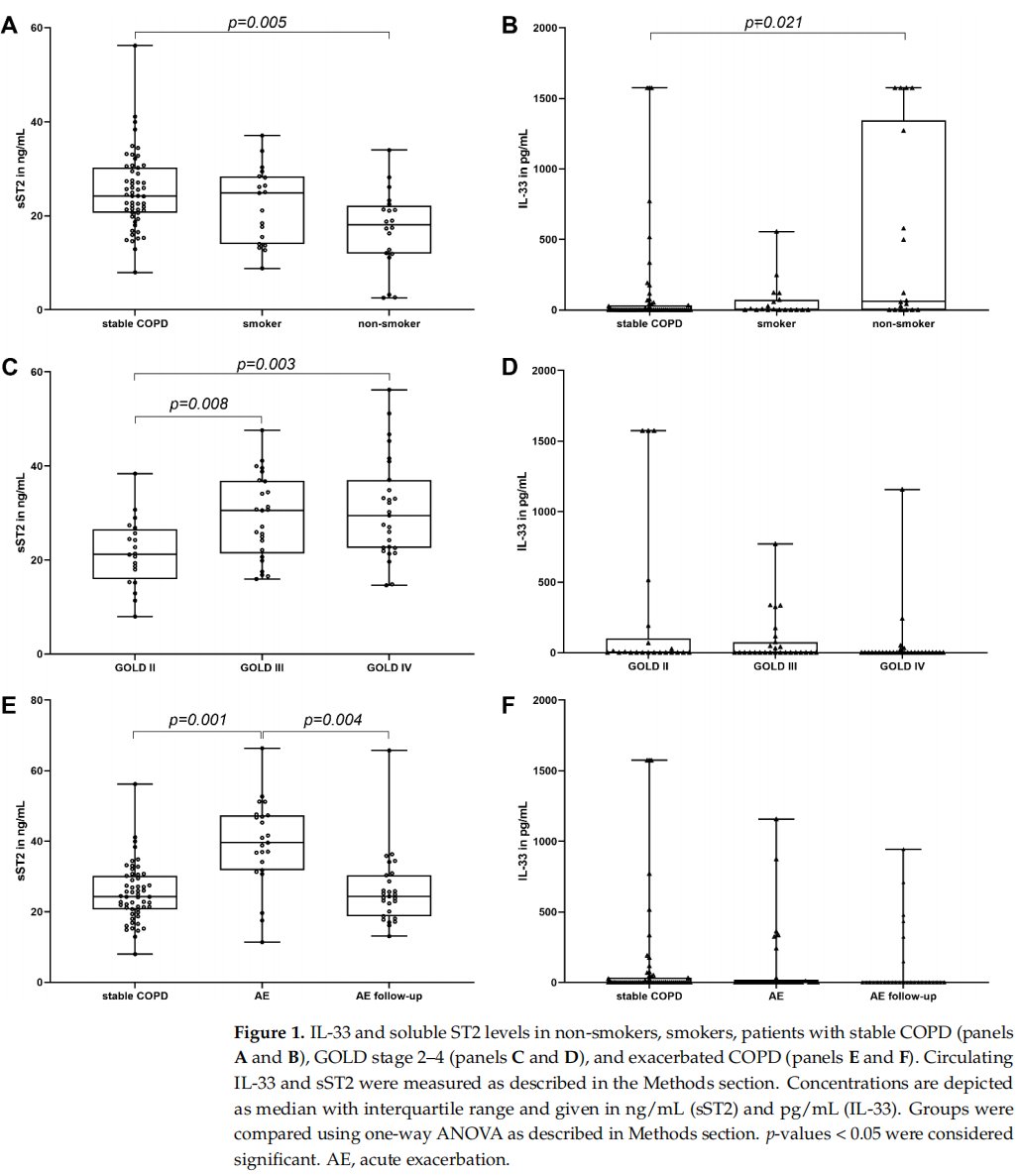
文章插图
FEV1%预计值与总样本中sST2呈负相关(图2A),sST2与总肺容量(图2B)、肺泡-动脉氧差(图2C)、吸烟史(图2D)、心率(图2E)呈显著的单因素相关。
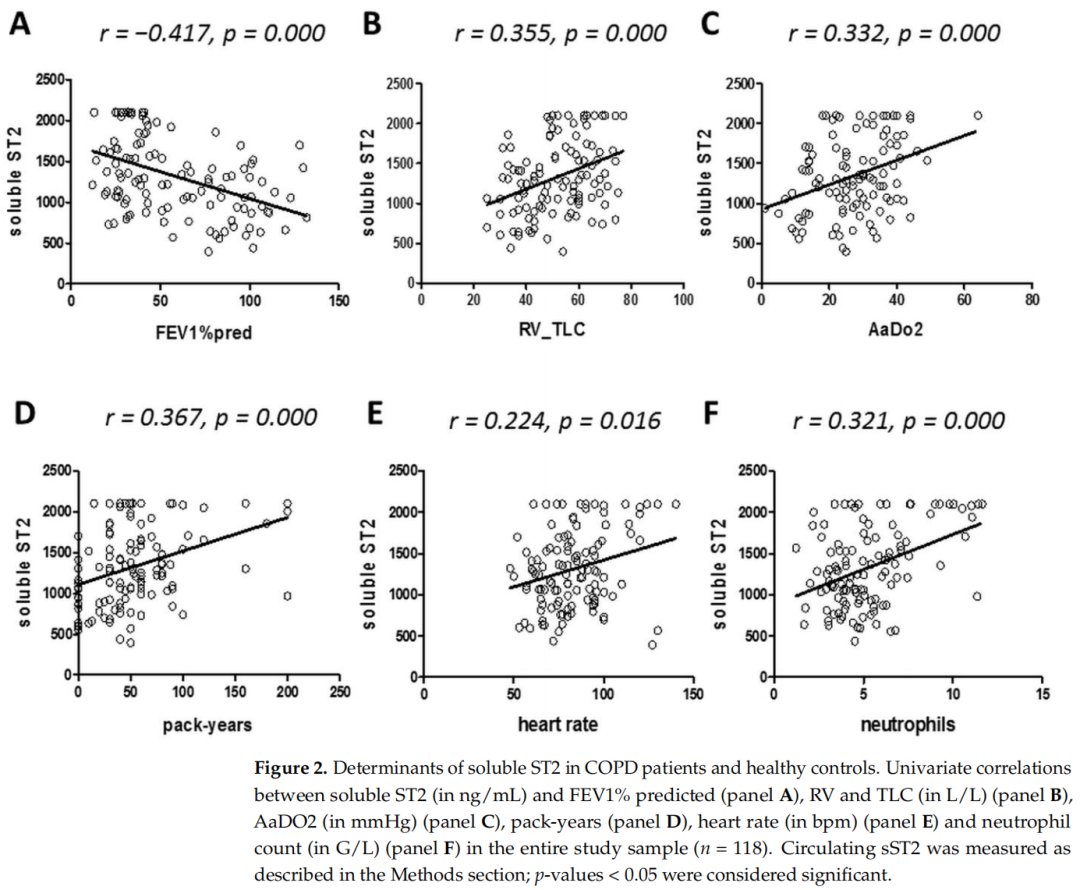
文章插图
在多因素分析中,可以发现收缩压、FEV1%预计值、吸烟史、中性粒细胞和LDH是sST2的独立预测因子,R2= 0.468(表2)。
3.3. sST2预测COPD死亡率
中位随访时间10.6年,死亡28例(47.5%)。其中20例(71.4%)死于COPD相关呼吸衰竭,4例(14.3%)死于肺恶性肿瘤,2例(7.1%)死于心血管死亡,2例(7.1%)死于肝硬化和肝功能衰竭。 Cox比例风险回归模型适用于评估sST2对全因死亡率的预测价值。在单因素Cox回归模型中,sST2是一个强有力的死亡率预测因子,HR/1-SD 3.9(95% CI 1.7-9.4,p=0.002,表3)。调整年龄和性别后,sST2独立预测全因死亡,HR/1-SD 3.9(95% CI 1.4-10.9,p=0.007)。进一步调整分组年限后,FEV1%预计值和CRP、sST2仍是全因死亡率的显著独立预测因子,调整后HR/1-SD 2.9(95% CI 1.1-8.4,p=0.035)。
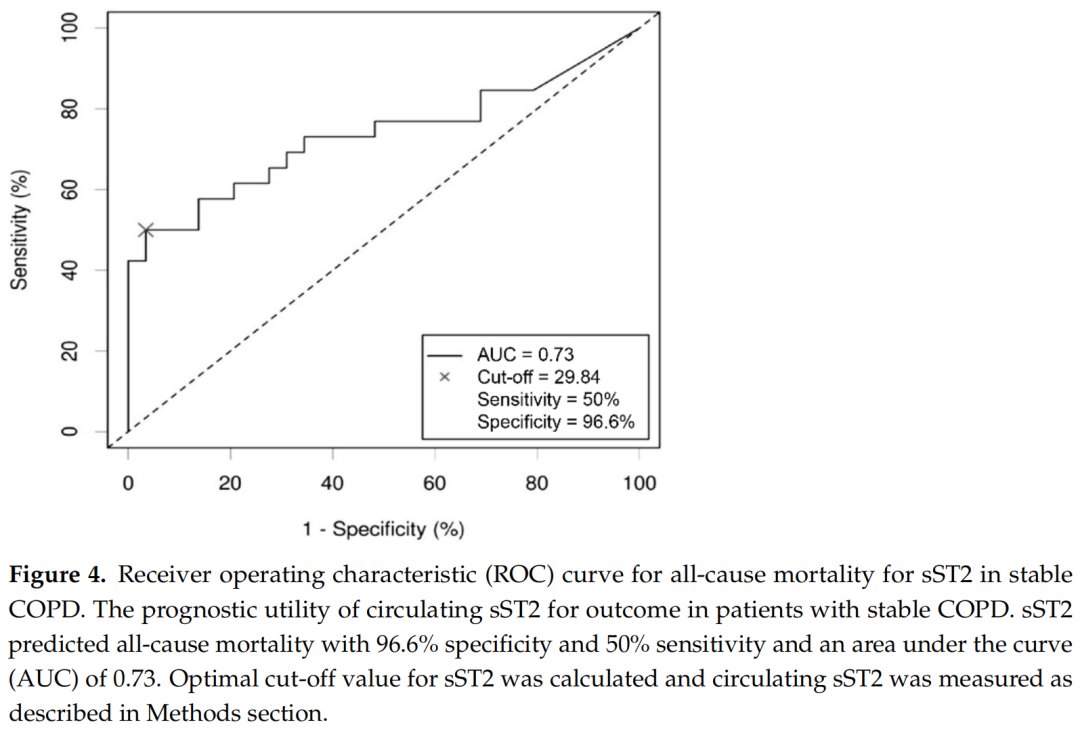
14例COPD患者(23.7%)的sST2均高于29.84ng/mL。在Kaplan-Meier生存曲线中,与临界值以下的sST2相比,临界值以上的sST2与更高的死亡率相关(log-rank:p<0.001,图3)。sST2预测死亡率的特异性为96.6%,敏感性为50%,AUC为0.73(图4)。
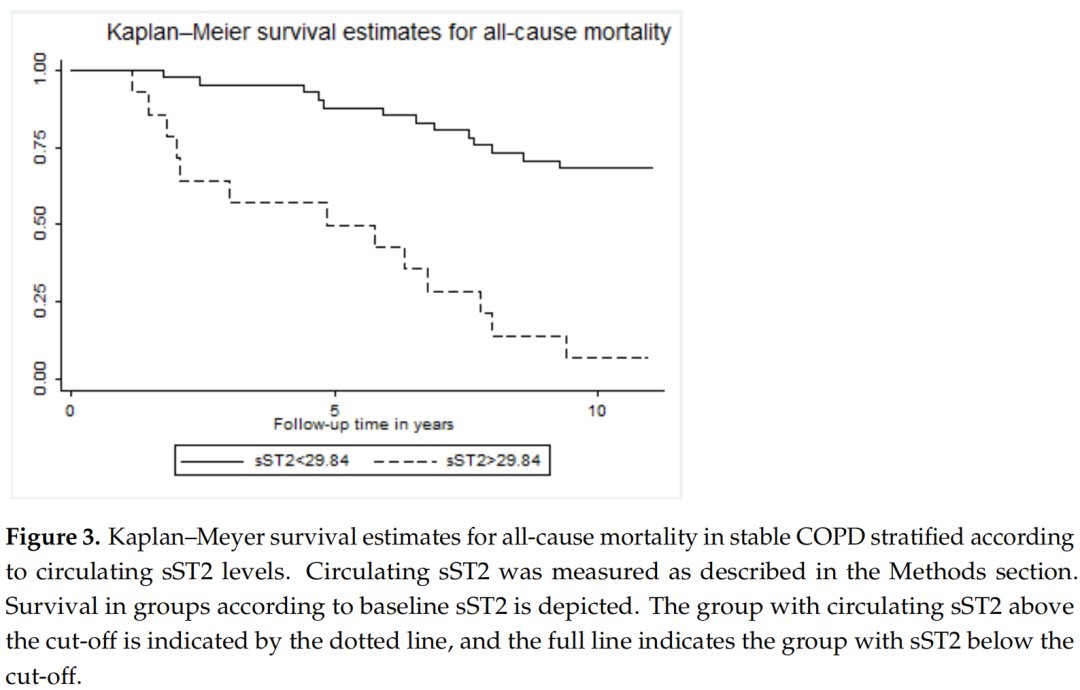
文章插图
文章插图
此外,在年龄、性别、吸烟史、FEV1%预计值和CRP的模型中加入sST2后,预测全因死亡率的Harrell’s C指数AUC从0.69(95% CI 0.59~0.80)提高到0.79(95% CI 0.71~0.87,p=0.036,表4)。
04
小结
目前对于COPD患者急性加重的诊断主要依据患者的症状及医生的主观判断,因此临床迫切需要一个高灵敏度、高特异度的客观标志物来指导诊疗。
IL-33高表达于肺组织细胞、气管壁内皮细胞等,在主动防御、炎症反应及免疫调节中均发挥重要作用。sST2作为诱饵受体,竞争性结合IL-33,阻断IL-33/ST2L的信号传导,减轻炎症反应。
本研究对COPD患者和健康对照者循环IL-33和sST2进行了调查。可以发现,COPD患者与健康对照者相比,sST2水平显著升高,IL-33水平降低。此外,sST2水平随疾病严重程度和COPD急性加重而升高,并与疾病的功能参数显著相关本研究可以首次证明 sST2是COPD长期全因死亡率的强有力的独立预测因子 ,并结合本组患者既定的临床危险因素改善危险分层。
研究结果表明,吸烟者和COPD患者循环IL-33水平较非吸烟者低。吸烟者循环sST2水平较高,且与吸烟史呈正相关。
此外,COPD患者IL-33浓度较低,且与疾病严重程度无关,与既往资料一致。值得注意的是,IL-33在近三分之二的COPD患者和72%的急性加重期患者中检测不到,低或无法检测的IL-33很可能是由高循环水平的sST2引起的。由于sST2是IL-33的诱骗受体,而IL-33可以诱导sST2的产生,因此可以推测COPD患者循环sST2增加反映了局部IL-33表达增加和肺部炎症反应加重。
总而言之,COPD患者循环sST2水平升高,IL-33水平降低,sST2浓度随气流阻塞程度增加而升高,且在COPD急性加重期达到峰值。 sST2可作为COPD患者独立的预后指标,可用于改善COPD患者的危险分层 。
这项研究有若干局限性。第一,样本量较小,没有按照GOLD ABCD方案对COPD患者进行分类;第二,根据本研究所提供的用于IL-33测定的ELISA生产厂家提供的资料,重组人ST2/Fc-嵌合体不产生交叉反应,但在浓度>12.5ng/mL时有干扰,而在本次研究中没有排除这种干扰;最后,排除了合并症,尤其是心血管疾病,这同时也加强了对COPD相关死亡率的解释。
【参考文献】 [1] Urban MH, Stojkovic S, Demyanets S, Hengstenberg C, Valipour A, Wojta J, Burghuber OC. Soluble ST2 and All-Cause Mortality in Patients with Chronic Obstructive Pulmonary Disease-A 10-Year Cohort Study. J Clin Med. 2021 Dec 23;11(1):56. doi: 10.3390/jcm11010056. PMID: 35011794; PMCID: PMC8745630. [2] 尹晶,陈文涛,郁毅刚.重症COPD患者IL-33/ST2比值与血气指标、氧化应激反应程度的相关性分析[J].分子诊断与治疗杂志,2020,12(03):305-308. [3] 张曙晴,张骆军,周小林,王玉蓉,沈晓雯.慢性阻塞性肺疾病患者血清IL-33、sST2、CRP水平与病情严重程度的相关性研究[J].中国实验诊断学,2021,25(11):1610-1613.
内容整理:北京利德曼市场部
图文设计:三度医学 CtrlZ
排版编辑:三度医学 Simin
责任编辑:三度医学 May
- 一日三餐|慢性胃炎有癌变的风险?别慌,积极做好6点可防癌变
- 慢性病|70岁后不宜运动,经常运动反不利于长寿,有道理吗?医生给出说明
- 健康|做好这四点,慢性肾脏病人开心、健康过春节
- 吸入性肺炎|年底聚会男子喝下1斤半白酒后呼吸衰竭住进ICU
- 支气管镜|醉酒伤肺?专家提醒,过量饮酒当心吸入性肺炎
- 慢性肉芽肿|世界防治麻风病日:麻风病可防可治 不可怕
- 维生素d|多补充维生素,帮你远离慢性病!日常这样吃,防缺乏,强体质,更健康~
- 咽喉|慢性咽炎总不好?中医有方法,自我调护学起来!
- 牛凯|慢性肾衰竭 有哪些症状?
- 慢性鼻炎|游泳体育干货丨锻炼时身体上发生突发事件处理办法
