疗法|Cell:促进免疫的纳米生物疗法抑制肿瘤生长和增强检查点抑制( 二 )
文章图片
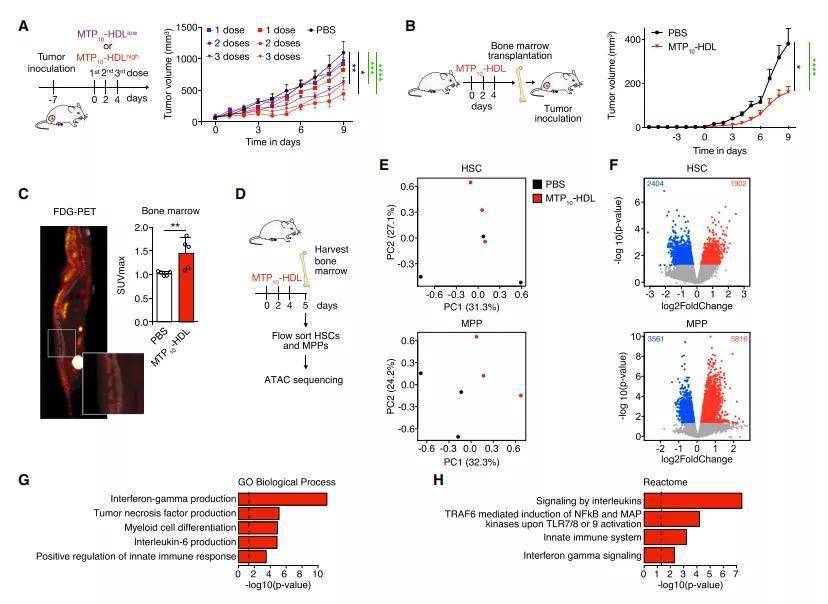
图3:MTP10-HDL治疗可抑制肿瘤生长并激活造血干细胞
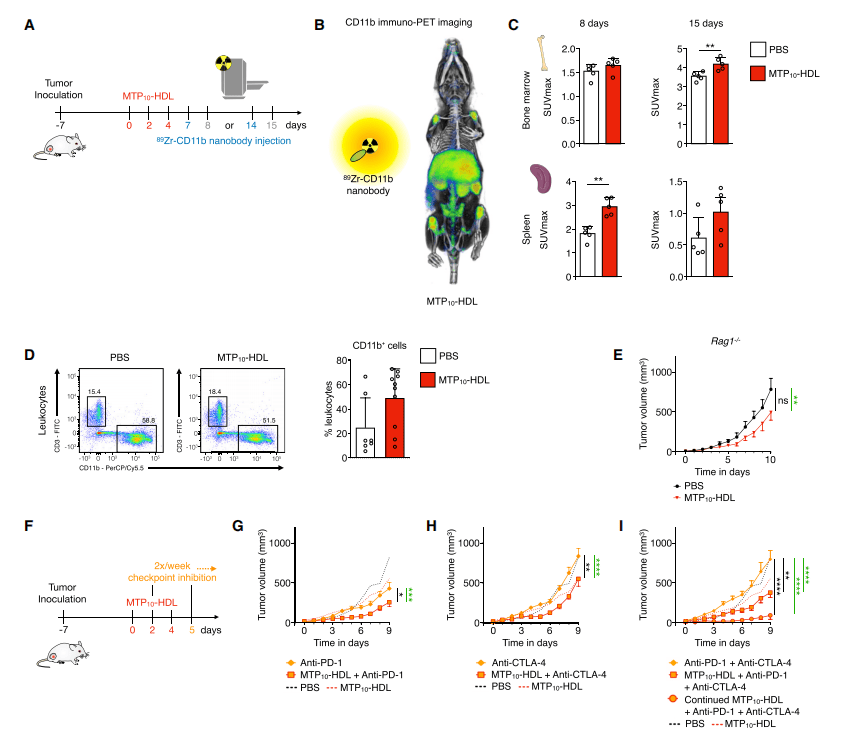
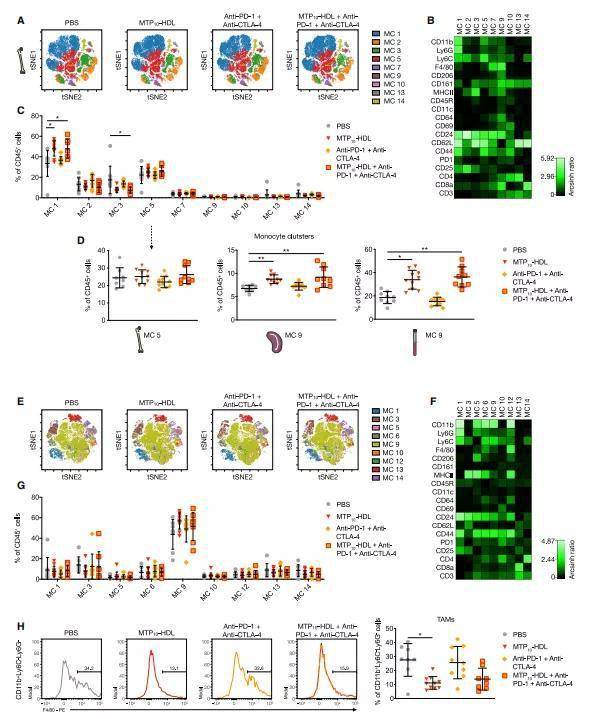
MTP10-HDL治疗导致HSC和MPP的表观遗传重组 , 并导致骨髓生成增加 , 这是一个特征(图3) 。 通过先进的成像技术 , 作者发现经过训练的免疫诱导的骨髓细胞生成引起了系统范围内骨髓细胞的快速和持久的增加(图5B和5C) 。 作者假设高度训练有素的单核细胞在肿瘤微环境促进抗原呈递细胞(信号1) 。 此外,作者的研究结果表明,骨髓细胞高反应性,训练免疫的另一个特点,提出了生产体外和体内细胞因子(3)信号(图1 f和4 e),作者也期望发生在肿瘤微环境产生影响 。 综上所述 , 这些因素可能增强检查点阻断免疫治疗的效果(信号2 , 图5F 5I) 。 癌症发生的另一个方面是存在免疫抑制细胞 , 如TAMs。 流式细胞术分析显示 , MTP10-HDL处理显著减少了TAM的种群(图5D和6H) , 这一结果有利于检查点抑制剂治疗 。 后一种变化 , 加上通过诱导训练免疫增加骨髓生成 , 可能是显著的肿瘤生长抑制背后的免疫学驱动力 。 许多其他类型的肿瘤 , 如多形性胶质母细胞瘤和胰腺癌 , 表现为免疫瘫痪或冷TME , 因此对免疫治疗不敏感 。 先天免疫激活通过训练免疫的结合可以用于治疗这些恶性肿瘤 , 特别是结合检查点抑制 。
文章图片
图5:诱导训练免疫增强检查点封锁疗法
文章图片
图6:经过训练的免疫引起向髓细胞的全身转移
作者精心设计的纳米生物平台包括表面功能化的高密度脂蛋白纳米盘 , 具有固有的生物相容性和高的体内耐受性 。 未功能化重组HDL的安全性已在心血管疾病试验中得到证实 。 MDP和MTP加入训练有素的免疫化合物 , 也有很好的耐受性 , 它们的毒性谱也得到了很好的研究 。 MTP10-HDL单药治疗没有影响肾功能、体重、行为和宏观特征 。 PET成像显示肝脏蓄积 , 血液化学检查未见毒性 , 肝脏形态保持不变 。 MTP10-HDL在非人类灵长类动物中的生物分布和毒性也被监测 。 重要的是 , 在这个平移模型中也记录到了一个类似的良好安全性剖面 。 因此 , 作者可以预见临床转译的直接途径 。 该平台的灵活性使其能够包含不同的MDP/MTP表面载荷 , 从而允许创建训练有素的促进免疫的纳米生物库 。
基于综合筛选 , 同时整合稳定性测量、体外训练免疫试验和体内生物分布研究 , 作者选择MTP10- HDL作为主要候选药物 。 作者使用综合RNA测序、流式细胞术和多种体内成像模式的广泛方法分析了MTP10-HDL的强抗肿瘤特性 。 MTP10-HDL抗肿瘤机制的深入研究促使作者将其与检查点抑制相结合 。 作者发现联合方案导致增强的抗肿瘤免疫反应 。 作者的研究为开发训练免疫诱导作为体内细胞疗法治疗癌症铺平了道路 , 无论是作为单一疗法还是与其他免疫疗法相结合 。
原文链接:https://doi.org/10.1016/j.cell.2020.09.059
- 央视新闻|商务部:RCEP将促进各方充分利用协定发展本国经济
- 互联网|医疗质量控制成互联网医疗行业“红绿灯”,三大环节促进线上医疗质量提升
- 梅奥诊所|【解读】梅奥诊所带你了解姜黄对乳腺癌的作用!最好的补充疗法来自于天然食物
- 细菌|CRISPR的诺奖是否发早了?Cell论文揭示细菌的另一种防御系统,具有基因编辑潜力
- 广安市中级人民法院,国兴公司|川渝两地法院联合发布民营经济保护典型案例 促进区域内法律适用标准统一
- 讲堂|武强中医院:健康讲堂 促进群众健康生活方式养成
- 延安日报|更新发展理念 补齐发展短板 促进新时代社会保障高质量发展 黄瑞芹
- 群众|南宁市中医医院:糖尿病义诊进基层健康促进惠民众
- 进行|Cell子刊:T细胞研究的新系统!单个血液干细胞可生成大量亚型和功能不同的T细胞
- 服务|企鹅杏仁集团与北京阳光易德签署战略合作协议,促进“心医疗” 承载大健康
