按关键词阅读:
【剂型|乙肝在研新药EDP-514,I期12月将完成,口服胶囊剂型】核苷酸类似物(NAs)比如 , 当前慢性乙肝一线药物恩替卡韦(ETV)、富马酸替诺福韦二吡呋酯(TDF)、富马酸替诺福韦艾拉酚胺(TAF)在药物学上又常被称为核苷逆转录酶抑制剂(NUC) , 正处于I期临床研究的EDP-514 , 将在评估核苷逆转录酶抑制剂(NUC)抑制的慢性乙肝病毒感染者中 , 进行28天口服EDP-514 , 以评估其安全性、耐受性、药代动力学和抗病毒活性(下图:来自生物制药公司Enanta Pharmaceuticals 药品研发管线) 。

文章图片
乙肝在研新药EDP-514 , I期12月将完成 , 口服胶囊剂型
值得注意的是 , 这种乙肝在研新药EDP-514的I期临床 , 首次发布时间:2019年7月5日 , 最新发布时间:2020年7月20日 , I期预计完成时间:2020年12月(临床试验编号:NCT04008004) 。 I期共分为两个部分 , 第一部分是随机、双盲、安慰剂对照研究 , 单剂量口服给药(EDP-514)评估其安全性(健康人上部分) 。 第二部分为随机、双盲、安慰剂对照研究 , 包括乙肝病毒感染者 。
第二部分主要是评估 , 已经使用核苷逆转录抑制剂(NUC)并获得抑制的慢性乙肝病毒患者的28天口服EDP-514 , 评估其安全性、耐受性、药代动力学和抗病毒活性(乙肝病毒感染者下部分) 。 这项乙肝在研新药第1期研究预计会在今年底完成 。 介绍一下 , EDP-514在健康人(上)和慢性乙型肝炎病毒感染(下)中的研究试验设计方法:
文章图片
这项I期研究预计纳入98名受试者 , 随机、序贯分配 , 掩蔽:四倍(参与者、护理提供者、研究者、结果评估者) , 也称为Ia/Ib期随机、双盲、安慰剂对照研究 , 评估健康受试者单次和多次递增剂量EDP 514的安全性、耐受性和药代动力学(上) , 以及核苷逆转录酶抑制剂(NUC)抑制的慢性乙肝病毒患者抗病毒活性感染(下) 。
这项I期临床已于2019年6月26日开始进行 , 将于今年2020年12月完成(距今较近) 。 手臂干预/治疗 , 实验组:EDP-514是一种口服胶囊剂型 , 受试者仅在第1天接受单剂量的EDP-514(SAD HV) , 从第1天到第14天开始每天给药一次EDP-514(MAD HV) , 或从第1天到第28天开始每天给药一次EDP-514(MAD HBV) 。

文章图片
安慰剂对照组:EDP-514 , HV SAD安慰剂组 , 配对安慰剂为口服一次给药 , 每日一次;安慰剂对照组:EDP-514 , HV MAD安慰剂组 , 匹配安慰剂为口服每日一次 , 持续14天 。 实验组:EDP-514 , HBV-MAD队列 , EDP-514第1、2、3剂量口服 , 每日一次 , 共28天 。 EDP-514是由生物制药公司Enanta Pharmaceuticals 研发 , 研究人员将关注本试验如下主要结果指标:
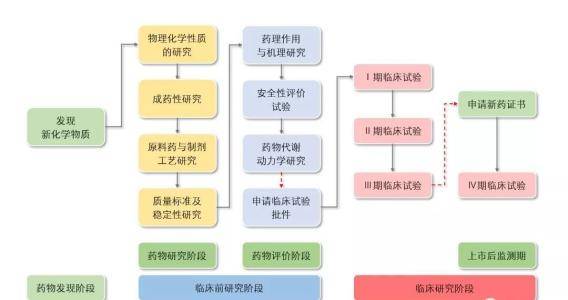
在HV SAD队列中最多8天时 , 通过不良事件以衡量安全性;在HV MAD队列中最多21天时 , 以不良事件衡量的安全性;HBV-MAD队列中最多56天时 , 通过不良事件衡量安全性(根据不同时间给药以了解研究药物EDP-514的不良事件发生情况) 。 次要结果指标:在HV SAD队列中最多6天 , EDP-514的Cmax、最长为51hV帧的第51d-4天队列;在HV MAD队列最长18天时 , EDP-514的AUC;HBV感染率高达28天时 , EDP-514的Cmax;在HBV-MAD队列中最多28天时 , EDP-514的AUC 。
文章图片
标准第1部分入选条件:受试者要签署并注明日期的知情同意书 。 年龄在18岁至65岁之间的健康男性或女性 。 排除标准:有临床相关的证据或病史;怀孕或哺乳期女性;在首次服用研究药物前7天内有发热病史 , 或受试者有活动性感染迹象;筛查或第1天尿药筛查呈阳性;目前吸烟或在筛查前3个月内使用过烟草;任何可能影响药物吸收的情况(如胃切除术、胆囊切除术);长期饮酒史等等 。 
稿源:(小番健康)
【】网址:http://www.shadafang.com/c/hn1023aWN2020.html
标题:剂型|乙肝在研新药EDP-514,I期12月将完成,口服胶囊剂型
