按关键词阅读:
安卓奎诺尔(Antroquinonol) , 是当前全球基于分子靶点:MEK-1蛋白激酶;Ras基因的一种治疗多领域在研新药 , 其中包括治疗非小细胞肺癌、胰腺肿瘤(I期);治疗非小细胞肺癌Ⅳ期、高脂血症、特应性皮炎、急性髓系白血病以及乙型肝炎病毒(II期)(下图来自:AdisInsight药物研发信息数据库) 。
文章图片
乙肝在研新药安卓奎诺尔 , II期探讨作用机制 , 2个剂量组进行
由中国台湾中山医学大学、黄金生物技术公司(Golden Biotechnology Corporation)主办的安卓奎诺尔II期完整试验设计方案 , 研究人员重点将关注安卓奎诺尔治疗慢性乙肝(CHB)的随机、安慰剂对照试验(临床试验编号:NCT04112147 ) 。 研究的主要目标是 , 评价安卓奎诺尔的抗乙肝病毒活性 , 次要目标是探讨安卓奎诺尔在CHB中的作用机制以及细胞因子的变化 。
安卓奎诺尔剂型为胶囊剂 , 实际II期研究开始时间:2018年8月10日 , 预计II期完成时间:2020年6月30日(此前普及为Antroquinonol的IIa部分) 。 这是一个II期、三臂、双盲、剂量范围、安慰剂对照试验 , 评价Antroquinonol对慢性乙肝患者的疗效 。 这项研究依据良好临床实践指南和赫尔辛基宣言进行的 。 从每个研究中心的当地伦理委员会或机构审查委员会获得批准 , 所有的慢性乙肝受试者均出具书面知情同意书(来自:美国临床试验数据库原研究人员评述 , 下图:安卓奎诺尔结构图) 。
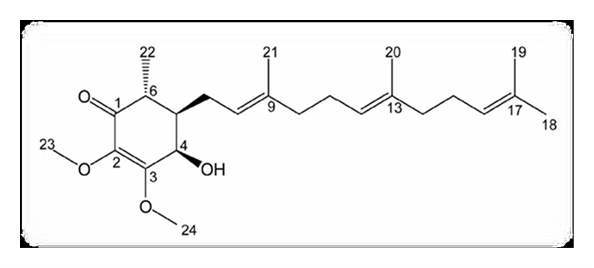
文章图片
II期完整试验设计如下:共纳入的60名慢性乙肝患者(每组20名)将接受Antroquinonol或安慰剂 。 每位受试者将接受1剂Antroquinonol或安慰剂 。 在开始筛查前 , 必须获得所有受试者的书面知情同意书 。 筛选期最长为14天 。 在完成所有筛选评估并确认合格标准以后 , 受试者会在第1天 , 每日服用100毫克、200毫克Antroquinonol或安慰剂 , 连续12周 , 直到有数据证明HBV-DNA大于10倍[最小值]、不可接受的毒性、不合规或受试者撤回同意 , 或研究人员决定停止治疗 , 以先到者为准 。
受试者将在第1天、第29天、第57天、第85天参与研究随访 。 研究人员根据评估时间表执行以下程序:体检、生命体征、临床试验测试、不良事件(AEs)伴随用药和受试者依从性 。 主要终点是 , 85天时乙肝表面抗原定量(logqhbsag)的变化 。 手臂干预/治疗 , 实验组:安卓奎诺尔胶囊100毫克 , 受试者将在12周内 , 服用50毫克BID安卓奎诺尔;药品:安卓奎诺尔胶囊100毫克 , 受试者将在12周内服用50毫克BID安卓奎诺尔 。

文章图片
实验组:安卓奎诺尔胶囊200毫克剂量组 , 受试者将在12周内服用100毫克BID安卓奎诺尔;药品:安卓奎诺尔胶囊200毫克 , 受试者将在12周内服用100毫克BID安卓奎诺尔 。 安慰剂对照品:受试者将接受为期12周的50毫克BID 安卓奎诺尔安慰剂 。 研究人员会关注安卓奎诺尔II期主要结果指标:0周和12周时 , 乙肝表面抗原定量(Log-qHBsAg) , 这也是本研究的主要目的 , 即主要终点:12周时的乙肝表面抗原定量的变化;
次要结果指标:第0周、第4周、第8周、第12周时 , 血清乙肝病毒DNA水平变化(即HBV-DNA以IU/mL计;第0周、第4周、第8周时 , 乙肝表面抗原的变化纤维化-4(FIB-4)量表 。 第0周、第12周与基线FIB-4量表相比的变化;第12周时 , 乙肝e抗原丢失率 , 即第12周HBeAg损失百分比;从第12周开始 , 谷氨酸草酰乙酸转氨酶(GOT)的基线变化;第12周与谷丙转氨酶(GPT)相比的变化 。 
稿源:(小番健康)
【】网址:http://www.shadafang.com/c/hn10119619102020.html
标题:变化|乙肝在研新药安卓奎诺尔,II期探讨作用机制,2个剂量组进行
