临床|每经数说丨8月下半月新药研发:拜耳1类心衰药物报上市,齐鲁再争托法替布缓释片首仿
_本文原题为 每经数说丨8月下半月新药研发:拜耳1类心衰药物报上市 , 齐鲁再争托法替布缓释片首仿
每经采访人员:金喆 每经编辑:魏官红

文章图片
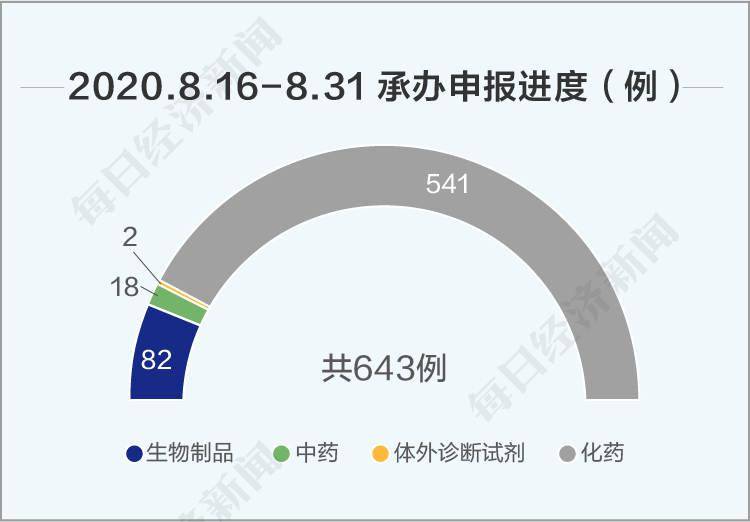
丁香园Insight数据库援引国家药品监督管理局药品审评中心数据显示 , 8月16日~8月31日 , 共承办643例申报进度 , 其中受理化药申请541项 , 生物制品申请82项 , 中药申请18项 , 体外诊断试剂2项 。
文章图片
《每日经济新闻》采访人员注意到 , 经过半个月“休整” , 本阶段药企重燃研发热情 , 新申报的药物研发数量回到6月、7月的水平 。 同时 , 我们可以在临床试验申报和上市申报的具体栏目中欣喜看到 , 越来越多跨国药企已经明显加快在中国市场的1类新药临床研发 , 或许不久之后我们在新药可及性上能比肩欧美日 。
与此同时 , 本土的创新药企也在提速 , 积极向港交所、科创板等资本市场靠拢 , 寻求更灵活的融资途径 。 而本次点评的德琪医药 , 已是港交所允许未盈利生物科技公司上市以来第30家“报名”的中国创新药企业 。
半月药闻
1、拜耳1类心衰新药Vericiguat片报上市 , 与欧美日同步
8月27日 , 拜耳提交1类新药Vericiguat片的上市申请 , 获得国家药监局受理 。
每经点评:
Vericiguat是首个开发用于治疗慢性心力衰竭恶化患者的可溶性鸟苷酸环化酶(sGC)激动剂 , 由拜耳和默沙东共同开发和推广 。 默沙东和拜耳在2014年建立了针对sGC的全球开发合作 。 二者合作开发的利奥西呱是首个上市的sGC调节剂 , 适应证是肺动脉高压 , 2019年全球销售额近10亿美元 。
今年7月16日 , 默沙东宣布FDA已经受理Vericiguat的新药上市申请 , FDA同时授予Vericiguat的上市申请优先审评资格 , PDUFA预定审批期限是2021年1月20日 。 今年6月 , 拜耳在欧盟和日本提交了Vericiguat的上市申请 。
Vericiguat如果获批上市 , 将是First-in-Class的sGC调节剂类心衰治疗药物 。 这意味着 , 该药在可及性方面 , 中国有望与欧美日同步 。
2、罗氏1类在研新药Tiragolumab在中国获批临床
【临床|每经数说丨8月下半月新药研发:拜耳1类心衰药物报上市,齐鲁再争托法替布缓释片首仿】8月25日 , 国家药监局药品审评中心公示 , 罗氏(Roche)旗下1类生物新药Tiragolumab获批临床试验默示许可 , 拟开发适应症为:与阿替利珠单抗联合治疗不可切除的局部晚期复发性或转移性食管鳞癌 。
每经点评:
Tiragolumab是罗氏开发的一款靶向T细胞免疫球蛋白和ITIM结构域蛋白(TIGIT)全人源化单克隆抗体 , 本次申请是Tiragolumab首次在中国获批临床 。
据了解 , 中国的食管癌发病和死亡率占到全球近一半 , 70%就诊时已属中晚期 , 一线治疗后预后差、后续治疗选择少 。 而在全球范围内 , Tiragolumab研发进度最快的处于三期临床研究阶段 , 分别针对非小细胞肺癌、小细胞肺癌 。
在中国 , 已有多家企业投入到TIGIT抗体的研发 , 获批临床的有信达生物的IBI939(一期在研)和百济神州的BGB-A1217(一期在研) 。 其中 , BGB-A1217在8月27日递交临床试验申请 , 目前正处于与PD-1抗体百泽安(替雷利珠单抗)联合针对癌症的1/2期临床开发阶段 。
今年7月 , 百济神州在投资者电话会议上重点介绍了4款自主研发的在研产品 , 其中就包括TIGIT抗体BGB-A1217 。 百济神州称 , 正在加速注册试验 。
目前 , 百济神州已在中国和澳大利亚启动一项BGB-A1217联合替雷利珠单抗用于治疗晚期实体瘤患者的1a/1b期临床试验 。 研究显示 , 该联合疗法一般耐受良好 , 无剂量限制性毒性(DLT) , 同时已经确定了联合疗法2期临床的推荐剂量 。
- 陈薇团队疫苗海外获批开展临床试验
- 数据宝|数说A股:芯片龙头市值蒸发超百亿元!大资金抢筹这些第三代半导体概念股
- 江南百景图兑换码使用次数说明 兑换码可以使用几次|江南百景图兑换码使用次数说明 兑换码可以使用几次
- 智通财经|信达生物(01801)第5款双抗申报临床
- 东方网|中国人脑图谱研究科创平台发布 科研及临床大设施逐步实现自主可控
- 中国临床营养网|【今晚直播】王兴国:减肥方法要个性化,营养师医师有话说!
- 全球医生组织|《NEJM·观察》欧洲心脏病学会临床研究成果和指南
- 针灸|专科录取进行时:一志愿口腔二志愿临床,结果被调剂到针灸推拿
- 北京|两款国产新冠灭活疫苗实物全球首次亮相,均已进入最后Ⅲ期临床试验阶段
- 上市|每经数说丨8月下半月新药研发:拜耳1类心衰药物报上市,齐鲁再争托法替布缓释片首仿
