有效性|辉瑞宣布新冠疫苗有效性 90%,全球首款 mRNA 疫苗要来了吗?( 三 )
注射后 , 三个疫苗组的志愿者都能在首次注射就产生新冠病毒的抗体 。 在低、中剂量组志愿者接种第二针后 , 抗体的滴度会再次上升 。 另外 , 志愿者体内能够测得 T 细胞产生的免疫应答 。
和其他技术路线疫苗横向对比 , 从目前几款完成了 II 期试验疫苗所公布的试验数据来看 , 不论技术路线是怎样的 , 所有新冠候选疫苗都能诱导出强烈的免疫应答 , 不良反应都在可控范围内 , 也都没有出现非常严重的不良反应 。 (阿斯利康和强生曾因为出现严重不良反应暂停试验 , 目前已恢复试验 。 详见: 刚刚!阿斯利康新冠疫苗恢复 III 期试验 , 此前因疑似严重不良反应叫停 )
具体来看 , 虽然 mRNA 疫苗的中和抗体滴度优于灭活疫苗及腺病毒载体疫苗 , 但 mRNA 疫苗的不良反应发生率比另外两款疫苗都高 。
这可能说明了 , mRNA 疫苗所激发的免疫反应更为强烈 , 但也同时导致了更多不良反应的发生 。 但具体是不是这个原因 , 还有待通过 mRNA 疫苗进一步的试验数据来完成相关研究 。
此外 ,Nature 昨夜的文章还提到 , 目前辉瑞疫苗呈现出的结果并不能回答所有的问题 。
宾夕法尼亚大学的疫苗学家 Paul Offit 说:「如果安慰剂组中出现了若干例重症的新冠感染者 , 那么更能表明疫苗预防的有效性 。 」
纽约市西奈山医学院的病毒学家 Florian Krammer 同时提到:目前疫苗虽然颇有成效 , 但仍然无法证明它能阻断病毒人与人之间的传播 。 而且 , 目前辉瑞所搜集的病例数比较少 , 还不能看出这款疫苗是否在不同人群间都能起到该有的保护效力 。
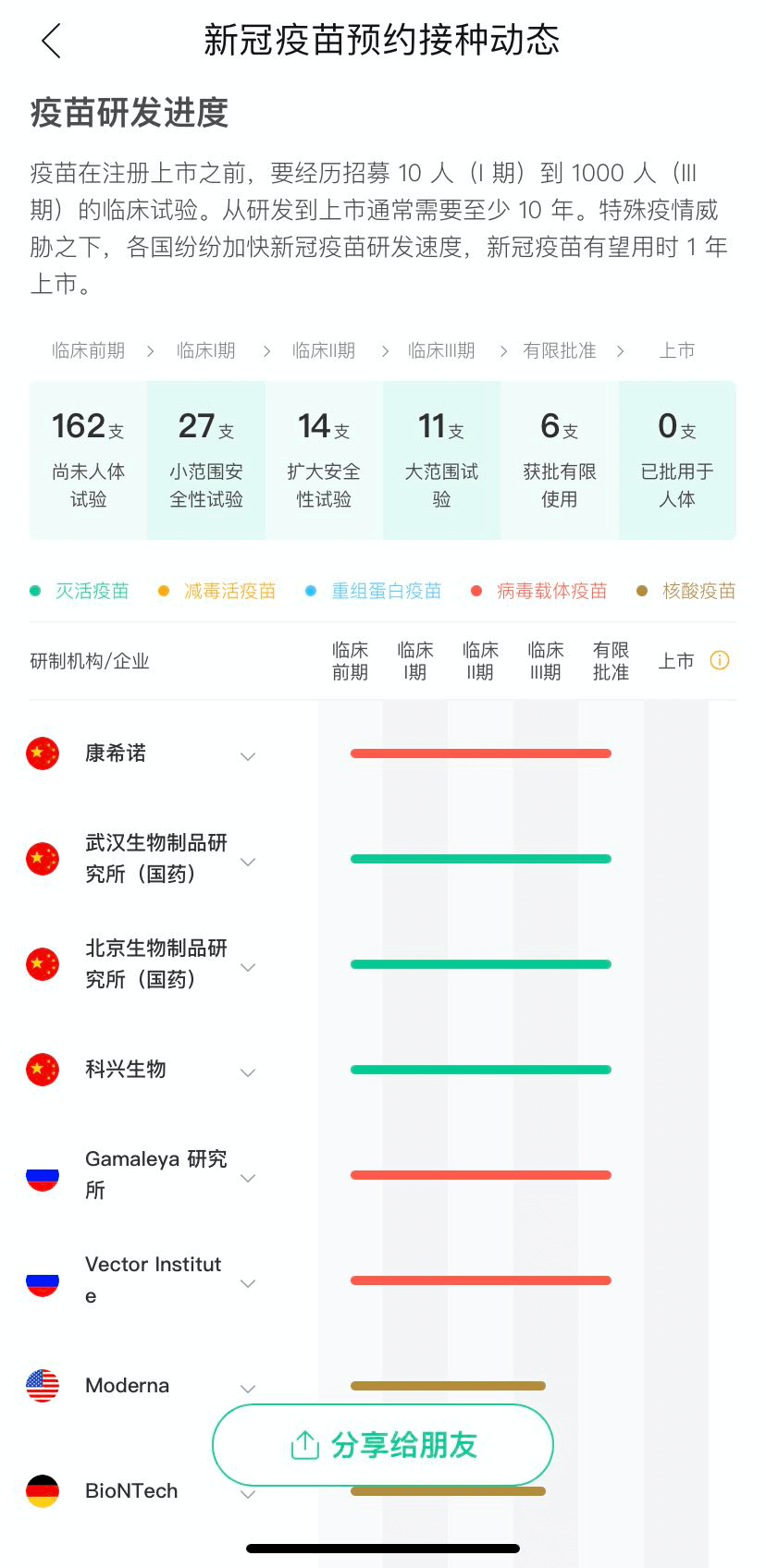
目前全球新冠疫苗的进度
截至 11 月 10 日 , 根据 WHO 官网公布的消息 , 全球共有 47 款新冠病毒候选疫苗进入临床试验阶段 , 较上次 WHO 公布数据新增 2 款 。
进入 III 期试验的为 10 款 , 其中中国 4 款(康希诺、国药北京和武汉、科兴)、英国 1 款(阿斯利康)、美国 4 款(辉瑞、ModeRNA、强生、Novavax)、俄罗斯 1 款(伽玛利亚) 。
另外 , 印度 Bharat 公司官方社交媒体称其疫苗的 III 期试验已获批 , 而 WHO 所公布的信息中 , 仍显示其 III 期试验暂未开展 。
文章图片
图源:来问丁香医生
总体来看 , 在当前人类与疫情的对抗中 , 辉瑞的这项结果给我们带来了新的希望 。 但也正因为这还是一项早期有效性数据 , 都还需要更长的时间来验证 。
就像庞麦郎在歌里唱的 , 只有时间才能给我们答案 。 (审核:gyouza)
致谢:本文经 北京生物制品研究会会员、知名健康博主 卤煮疫苗 专业审核
题图来源:图虫创意
参考资料:
1)
https://www.pfizer.com/news/press-release/press-release-detail/pfizer-and-biontech-announce-vaccine-candidate-against
2)Mulligan, M.J., Lyke, K.E., Kitchin, N. et al. Phase I/II study of COVID-19 RNA vaccine BNT162b1 in adults. Nature 586, 589–593 (2020).
3)Sahin, U., Muik, A., Derhovanessian, E. et al. COVID-19 vaccine BNT162b1 elicits human antibody and TH1 T cell responses. Nature 586, 594–599 (2020).
4)
https://www.pei.de/SharedDocs/Downloads/EN/newsroom-en/dossiers/ppt-erste-studie-sars-cov-2-impfstoff-en.pdf?__blob=publicationFile&v=7
6)
https://www.who.int/publications/m/item/draft-landscape-of-covid-19-candidate-vaccines
丁香园期待你的来稿!
好文不怕贵 , 舍得给稿费
投稿邮箱:tougao@dxy.cn
后台回复「投稿」即可查看投稿规则
- 诺基亚3.4|诺基亚3.4/2.4发布时间宣布:预计将于11月26日亮相
- 私生饭|无预警宣布“我要休学” 小哈利上传自拍揭真相
- 新冠疫苗|新冠疫苗之王诞生?有效性94%,明年生产10亿剂!周期资产狂飙
- 吾事通说|芯片又有“好消息”?中芯国际宣布“新突破”,芯片国产化或提速
- tvb|再度离巢!28岁港姐小花宣布离开TVB,名校毕业家住4000万豪宅
- 疫苗|我国新冠疫苗研发,和美国辉瑞差距有多大?看看钟南山院士怎么说
- 疫苗|复星医药和 BioNTech宣布mRNA候选疫苗BNT162b2 获中国国家药监局临床试验批准
- moderna|又一款新冠疫苗来了!Moderna三期试验疫苗有效性为94.5%
- 华为|卖了!华为出售荣耀17号宣布,30家供应链厂商接盘
- 澎湃新闻|超越辉瑞!美国莫德纳称其新冠疫苗有效率94.5%
