Mordor报告:诺华、GSK、卢米纳或驱动PBC治疗市场年增长超10%
2020年3月6日 , 知名市场分析机构Mordor Intelligence发布了一篇名为《原发性胆汁性胆管炎(PBC)疗法市场预测2020-2025》的调研报告 , 通过分析PBC药物的研发现状 , 预测其未来5年的市场走势 。 目前 , 身处这一赛道的关键企业包括:诺华(Novartis) , 葛兰素史克(GSK) , 卢米纳制药(Lumena Pharmaceuticals) , 梯瓦制药(Teva Pharmaceuticals) , 吉利德(Gilead)等 。
文章图片
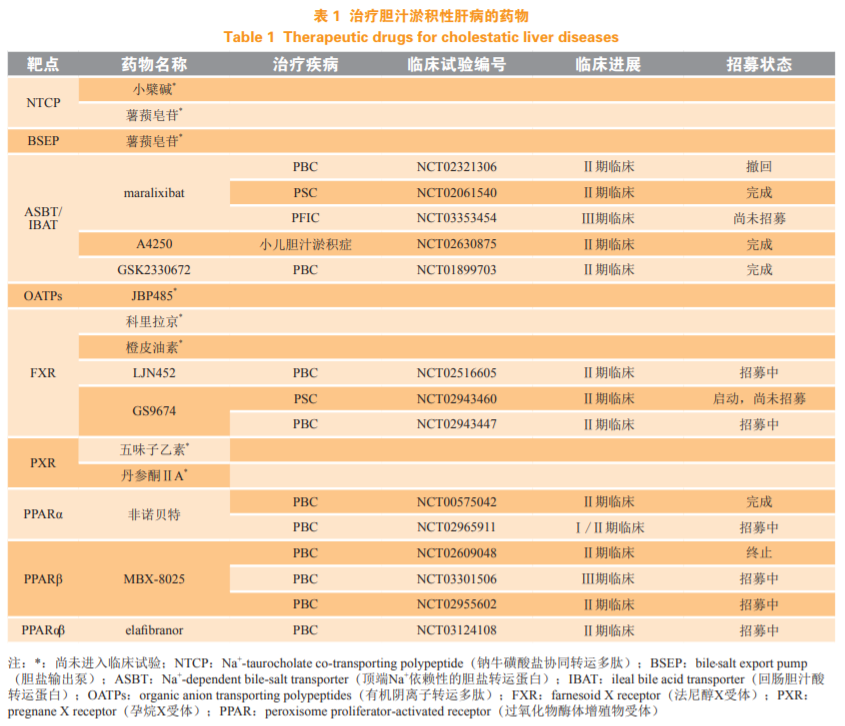
PBC是一种罕见的慢性肝脏疾病 , 患者体内胆管损伤积累 , 导致胆汁淤积、肝纤维化甚至肝硬化 , 最终发展为肝功能衰竭 。 目前 , 国际上主要采用熊去氧胆酸(UDCA)或奥贝胆酸(OCA , 主要用于对UDCA应答不敏感患者)进行对症治疗 , 晚期患者则只能通过肝移植来延长生存期 , 这也是导致美国女性接受肝移植的首要病因 。 为此 , 诺华、GSK、卢米纳等企业纷纷奔跑进场 , 由此打开了一场研发竞速 。
文章图片
诺华(Novartis)
诺华开发的Tropifexor是一种新型、高效的FXR激动剂 , FXR即法尼醇受体 , 在胆汁酸代谢及胆固醇代谢中发挥重要作用 。 有研究证明 , 该药物可逆转由胆汁酸蓄积导致的胆汁淤积性肝损伤 。
2019年12月 , 美国临床药理学院(ACCP)在官网公开了关于Tropifexor在健康志愿者中的临床试验报告 , 报告显示Tropifexor在其有效剂量范围内 , 均表现出良好的药物安全性及耐受性 。
葛兰素史克(GSK)
GSK研发的GSK2330672(利尼昔巴特)是一种回肠胆汁酸转运蛋白(IBAT)抑制剂 , 主要用于治疗PBC引发的瘙痒症 。

文章图片
2017年2月 , 《柳叶刀》公开了英国Newcastle生物医学研究中心的Vinod等应用GSK2330672治疗PBC瘙痒症患者的Ⅱa期临床试验报告 。 报告显示 , 在给药14 天后 , 患者皮肤瘙痒评分下降 57% , 血清中总胆汁酸含量减少 50% , 表明该药物具有一定的PBC治疗效果 , 且无严重不良反应 。
卢米纳制药(Lumena Pharmaceuticals)
卢米纳制药旗下针对罕见肝病的药物Maralixibat(LUM-001)曾在2014年被英国夏尔(Shire)买入 。 随后 , 一项关于Maralixibat治疗 PBC 的Ⅱ期临床试验表明 , 该药物能缓解 PBC 患者的皮肤瘙痒症 , 但同时表现出明显的副作用 , 而被夏尔终止试验 。
2016年 , Maralixibat迎来了关键的转折点 , 其在治疗PFIC(进行性家族性肝内胆汁淤积症)时打出了一记重拳:研究显示 , 该药物能有效抑制胆汁酸在回肠的重吸收 , 促进胆汁酸随粪便排出体外 , 目前已被美国FDA认定为新药突破性疗法 , 正处于Ⅲ期临床试验阶段 。 后续 , 不排除将其再用于PBC联合用药研究 。
文章图片
吉利德(Gilead)
吉利德旗下的GS-9674 是人工合成的 FXR 激动剂 , 其通过抑制胆汁酸合成减轻胆汁淤积性肝损伤 。
2018年AASLD年会上 , 吉利德公布了GS-9764治疗PBC的Ⅱ期临床数据 。 数据显示 , 患者用药后 , 肝脏生化及胆汁淤积标志物得到显著改善 。
【Mordor报告:诺华、GSK、卢米纳或驱动PBC治疗市场年增长超10%】诺华、GSK、卢米纳、吉利德的入场 , 开启了“后奥贝胆酸”时代 , 为打破部分患者应答不敏感而“无药可医”、“副作用明显”等现象提供了巨大的可能性 。 该报告预测 , 基于全球PBC发病率上升以及各大龙头研发投入的聚拢 , 2020至2025年PBC治疗市场的年复合增长率有望达到10% 。
- 报告|7月钢铁PMI:生产增速有所回落,市场需求仍相对偏紧
- 报告|北京连续4日“零新增”
- 详情公布!广州市报告新增境外输入确诊病例1例
- 成都发布|成都报告1例境外输入无症状感染者,轨迹公布
- 成都发布|轨迹公布,成都报告1例境外输入无症状感染者
- 印度_社会|死亡98人!快速火化、不敢报告死讯
- 报告|北京8月2日无新增确诊病例 连续4日零新增
- 确诊|山东新增境外输入确诊病例2例:烟台报告,来自菲律宾
- 成都报告1例境外输入无症状感染者,轨迹公布
- 报告|死亡98人!快速火化 印度这起假酒案不简单
