突破!国内首款,这家龙头公司旗下CAR-T细胞疗法获批临近
**《科创板日报》(上海 , 采访人员 徐红)讯 据《科创板日报》采访人员获悉 , 复星医药(600196.SH)旗下复星凯特CAR-T产品益基利仑赛注射液(代号FKC876 , 抗人CD19 CAR-T细胞注射液)目前已完成三合一审评 。
根据新药审评流程 , 三合一审评结束后 , 仅剩国家药监局药品审评中心形成报告、递交国药监签字等手续 。 这意味着 , 这款CAR-T细胞治疗产品离获批仅一步之遥 , 有望成为国内首款上市CAR-T疗法 。
益基利仑赛注射液即吉利德子公司Kite制药的抗人CD19 CAR-T细胞注射液(商品名Yescarta) 。 复星凯特从Kite Pharma引进Yescarta , 获得其在中国的技术及商业化权利 , 并于中国境内(不包括港澳台地区)进行本地化生产 。
2020年2月24日 , 复星医药曾发布公告 , 宣布FKC876的上市申请获国家药监局受理 , 用于治疗成人复发难治性大B细胞淋巴瘤 , 包括弥漫性大B细胞淋巴瘤(DLBCL)非特指型、原发性纵隔 B 细胞淋巴瘤(PMBCL)、高级别B细胞淋巴瘤和滤泡淋巴瘤转化的 DLBCL 。
截至目前 , 除了复星凯特的益基利仑赛注射液以外 , 药明巨诺的瑞基仑赛(研发代码为JWCAR029)亦已在2020年6月申报上市 。 这是继复星凯特之后 , 国内第二款申报上市的CAR-T细胞疗法 。
同FKC876类似 , JWCAR029是在美国巨诺公司旗舰产品JCAR017基础上 , 由药明巨诺自主开发的CAR-T产品 , 本次申报适应症预计为复发难治性B细胞非霍奇金淋巴瘤 。
公开信息显示 , 迄今为止 , 全球共有三款已上市的CAR-T类免疫细胞治疗药物 , 其中诺华的Kymria和Kite公司的Yescarta均于2017年获批 。 之后 , 时隔近3年 , FDA于2020年7月24日再次批准了一项新的CAR-T细胞疗法上市 , 即Kite公司的CD19 CAR-T细胞疗法Tecartus?(KTE-X19) , 用于治疗复发或难治性套细胞淋巴瘤(r/r MCL) 。
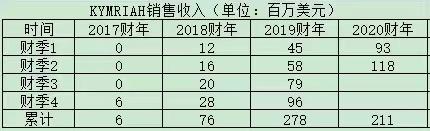
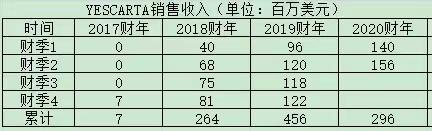
值得指出的是 , Kymria及Yescarta上市后 , 虽然两者的市场销售连年上升 , 但总的来说 , 并没有达到市场此前预期的“重磅炸弹药物”的目标 。 其中 , Kite公司的Yescarta整体表现要好于诺华的Kymria 。
市场分析认为 , 生产产能不足是限制销售的主要因素之一 , 而产能的差别也是导致这两款产品上市表现差异的重要原因 。 Yescarta在早期开发和申请上市过程中 , 产能问题相对解决得较好 , 因此拥有“先发”优势 。
 文章插图
文章插图
 文章插图
文章插图
图|诺华Kymria和Kite公司的Yescarta上市后销售走势与此同时 , CAR-T产品高昂的价格将许多患者挡在了“门外” 。 以Kymriah和Yescarta为例 , 两者的售价分别高达47.3万美元和37.3万美元 , 折合人民币均在300万上下 , 而这仅仅是药品的价格 , 整个治疗的总费用还不止这些 。
【突破!国内首款,这家龙头公司旗下CAR-T细胞疗法获批临近】那么 , 益基利仑赛注射液获批上市后又会如何定价?对此 , 据《科创板日报》采访人员了解 , 目前复星凯特内部虽已有多个定价方案 , 但最终的定价仍待落定 。 “总体来说 , 由于成本较高 , 因此不会太便宜 。 ”复星凯特相关高层表示 。
- 国内综艺喜欢小孩,国外代孕分手弃子,郑爽何时退圈?
- 《山海情》张嘉译闫妮状态突破,黄轩演技好,网友:这才是演员
- 《封神榜》土行孙,被誉为国内最知名矮星,现惨淡靠低保度日
- “救命药”上新!首款国产神经内分泌瘤新靶向药今日全国首批发货
- 手术|20岁高度近视小伙5分钟“告别眼镜”江苏省人民医院全飞秒激光手术半年内突破1000例
- 新突破:这一技术可有效分流心衰患者的心脏压力
- 青岛实现’零’的突破!青大附院获批建设省级临床医学研究中心
- 40年33个影帝,他是国内顶级男演员,演艺圈地位秒杀陈道明
- 青岛市省级临床医学研究中心取得零突破
- 心突破!心跨越!怀化市二医院成功开展心脏左束支起搏器植入术
