(健康时报采访人员 赵萌萌)1月11日,国家药监局网站公告称,即日起停止莲必治注射液在国内的生产、销售、使用,并注销其药品注册证书。公告表示,已上市销售的产品,由药品上市许可持有人负责召回,召回产品由所在地省级药品监督管理部门监督销毁或者依法采取其他无害化处理等措施。
据采访人员了解,这是首个被国家药监局下文停止产销的中药注射剂,在公告中提到,“根据《中华人民共和国药品管理法》第八十三条等有关规定,国家药品监督管理局组织对莲必治注射液开展了上市后评价”,本次公布的决定也是经评价后的结果。
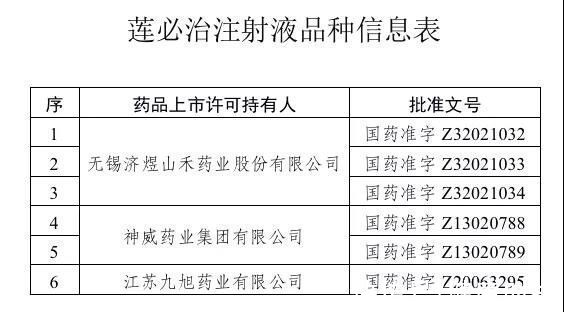
据了解,莲必治注射液是一种中药注射剂,具有清热解毒、抗菌消炎作用,主要用于细菌性痢疾,肺炎,急性扁桃体炎的治疗,该药在临床中多作为辅助用药,与其他抗菌药物合用。据据国家药监局,此前国内有莲必治注射液批准文号的企业有三家,分别是:无锡济煜山禾药业股份有限公司、神威药业集团有限公司、江苏九旭药业有限公司。
文章插图
“莲必治注射液被取消注册主要是由于不良反应较严重,而且没有搞清楚不良反应产生的原因。”北京中医药大学中药药理系主任、国家中医药管理局重点学科带头人孙建宁教授在接受健康时报采访时表示。
采访人员了解到,早在2006年,原国家食药监局就曾要求其修订说明书,注明:老年人、儿童、孕妇、哺乳期妇女及有肾脏疾病的患者应慎用。2017版国家医保目录又对其使用做了严格的限制,限二级及以上医疗机构使用。
【 双黄连注射液|中药注射液首次被退市,不良反应“尚不明确”现象将终结?】一直以来,中药注射剂的有效性、安全性问题就饱受争议,并且在近年来受到越来越严格的监管,包括修改说明书、医保报销受限、重点监控目录等。国家相关部门也越来越重视中药注射剂的安全性问题。
2018年,国家药监局曾发布公告,在临床已应用70多年的中药注射剂、儿科的常用药的柴胡注射液,因不良反应等原因,被禁用于儿童。同年,双黄连注射液也被要求增加警示语“本品不良反应包括过敏性休克”,同时4周岁及以下儿童禁用。
在2021版医保目录中,双黄连注射液、清开灵注射液、热毒宁注射液、鱼腥草注射液等40个中药注射剂被限二级以上医疗机构使用。
本次国家药监局出手注销文号,对于中药注射剂意味着什么?孙建宁教授解释,“除非发现严重不良反应,大批中药注射剂并不会被取消注册,但是会要求已上市中药注射剂尽快补充完善说明书中“禁忌”“不良反应”“注意事项”等相关内容,做到与化药说明书一样的细化。”
- 双方|LOL-LPL:Tarzan盲僧回旋踢一脚定乾坤,LNG 2-1击败FPX取得五连胜
- 双方|昔日温情不在,Theshy手刃老队友Rookie!WBG击败V5拿下三连胜
- 双枪|《幻塔》白月魁怎么配武器?高玩推荐“连携速切流”,全程伤害不断
- 潇潇|浙江双胞胎姐妹咳嗽一年四处求医,福州这家医院揪出病因,让人大吃一惊
- 特惠价|PS港服开启新春特惠:低至2折 生化8、双人成行半价
- 抑郁|情绪时而亢奋时而低落?心情就像过山车?你可能得了双相情感障碍……
- 李双庆|完美健康生活|春节将至,华西专家提醒你:胡吃海塞要不得!
- 障碍|眼见他喜欲狂,眼见他泪满裳?是双相情感障碍
- 肺栓塞|腿上出现青色“小蚯蚓”,有致命风险!3个动作轻松护双腿,赶紧学起来
- 单抗注射液|国家药监局:奥木替韦单抗注射液获批上市
